MS unter der Lupe
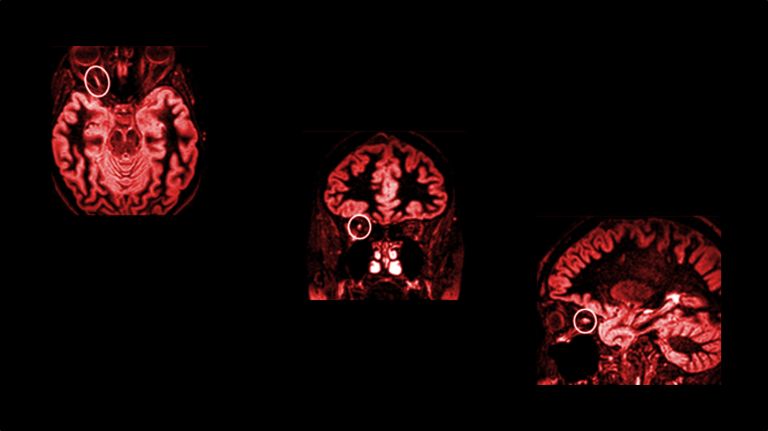
Die Multiple Sklerose – die Narbenbildung im Gehirn – geht auf die Schädigung von Axonen zurück: sie bildet die Basis der vielfältigen neurologischen Symptome.
Wissenschaftliche Betreuung: Prof. Dr. Hans-Peter Hartung, Dr. Melanie Schütte
Veröffentlicht: 15.08.2025
Niveau: mittel
- Verstreute Entzündungsherde im Gewebe des Gehirns und des Rückenmarks sind typisch für die Multiple Sklerose.
- Betroffen sind vor allem die Sehnerven, das Rückenmark, der Hirnstamm und das Marklager um die Ventrikel.
- Die Symptome sind eine Folge geschädigter Nervenhüllen und im Verlauf auch der Nerven selber abhängig vom Ort der Schäden.
- Für den schubförmigen Verlauf stehen effektive Medikamente zur Verfügung.
Hirnstamm
Hirnstamm/Truncus cerebri/brainstem
Der „Stamm“ des Gehirns, an dem alle anderen Gehirnstrukturen sozusagen „aufgehängt“ sind. Er umfasst – von unten nach oben – die Medulla oblongata, die Pons und das Mesencephalon. Nach unten geht er in das Rückenmark über. Er ist ein Zentrum lebenswichtiger Funktionen wie der Atmung und des Herzschlags und beinhaltet auf- und absteigende Bahnen zwischen Großhirn, Kleinhirn und Rückenmark.
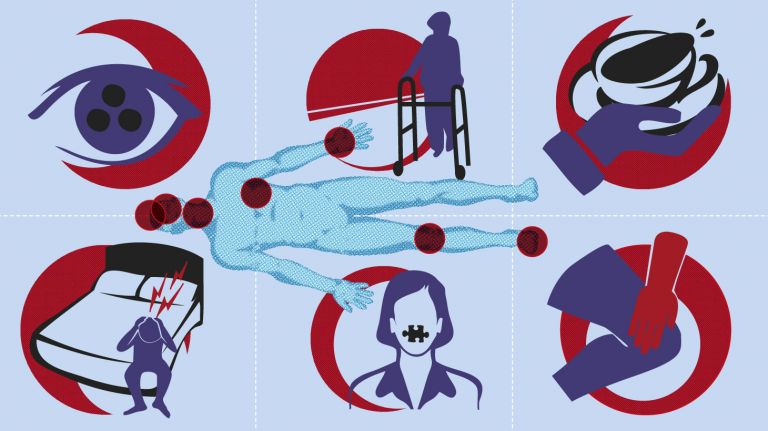
Abhängig vom Ort – Gehirn oder Rückenmark – und vom Ausmaß der Schädigung fallen die Symptome sehr unterschiedlich aus. Die typische Optikusneuritis ist oft der erste Schub einer MS, sie tritt bei 40 Prozent der Betroffenen auf.
Beschädigte Nervenfasern des Hirnstammes können eine Trigeminusneuralgie hervorrufen, eine Lähmung der Augenmuskeln und Doppelbilder. Sind die Nerven entzündet, die die Gesichtsmuskulatur versorgen, kann eine Gesichtslähmung auftreten. Schwindel und Brechreiz entstehen, wenn Nervenbahnen beschädigt sind, die die Verbindung zum Gleichgewichtsorgan herstellen. Entzündungsherde im Hirnstamm können auch zu einer verwaschenen Sprache führen.
Sind Nervenfasern im Kleinhirn oder seinen Verbindungsbahnen betroffen, führt dies zu Störungen in der Bewegung oder beim Stehen, abgehackter Sprechweise oder überschießenden Bewegungen. Sind Fasern im Rückenmark beschädigt, löst das sensorische Störungen (Kribbeln, Taubheitsgefühle) und motorische Störungen aus.
Die Muskeln können entweder erschlaffen oder verkrampfen. Weitere Beschwerden sind Blasen- und Mastdarmstörungen, Harnträufeln und Harndrang oder der Verlust über die Kontrolle der Harnblase oder des Darms. Durch Spastiken, Inkontinenz oder Gefühlsstörungen kommt es bei vielen MS-Betroffenen auch zu sexuellen Problemen, die sich in Libidoverlust, mangelnder Orgasmusfähigkeit oder Potenzverlust äußern können.
Rückenmark
Rückenmark/Medulla spinalis/spinal cord
Das Rückenmark ist der Teil des zentralen Nervensystems, das in der Wirbelsäule liegt. Es verfügt sowohl über die weiße Substanz der Nervenfasern, als auch über die graue Substanz der Zellkerne. Einfache Reflexe wie der Kniesehnenreflex werden bereits hier verarbeitet, da sensorische und motorische Neuronen direkt verschaltet sind. Das Rückenmark wird in Zervikal-, Thorakal-, Lumbal und Sakralmark unterteilt.
Hirnstamm
Hirnstamm/Truncus cerebri/brainstem
Der „Stamm“ des Gehirns, an dem alle anderen Gehirnstrukturen sozusagen „aufgehängt“ sind. Er umfasst – von unten nach oben – die Medulla oblongata, die Pons und das Mesencephalon. Nach unten geht er in das Rückenmark über. Er ist ein Zentrum lebenswichtiger Funktionen wie der Atmung und des Herzschlags und beinhaltet auf- und absteigende Bahnen zwischen Großhirn, Kleinhirn und Rückenmark.
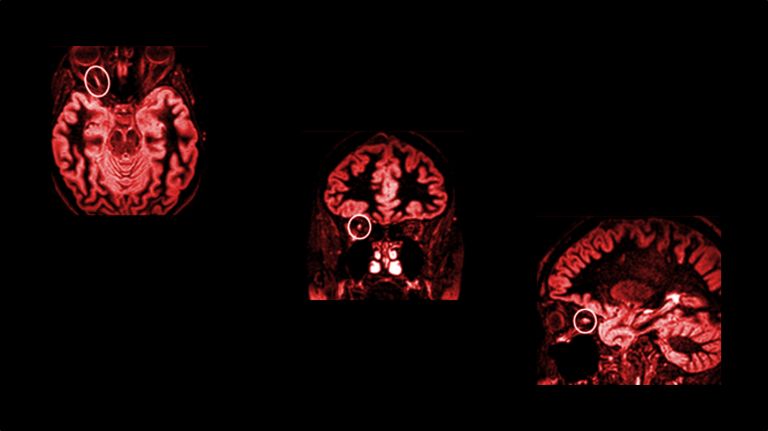
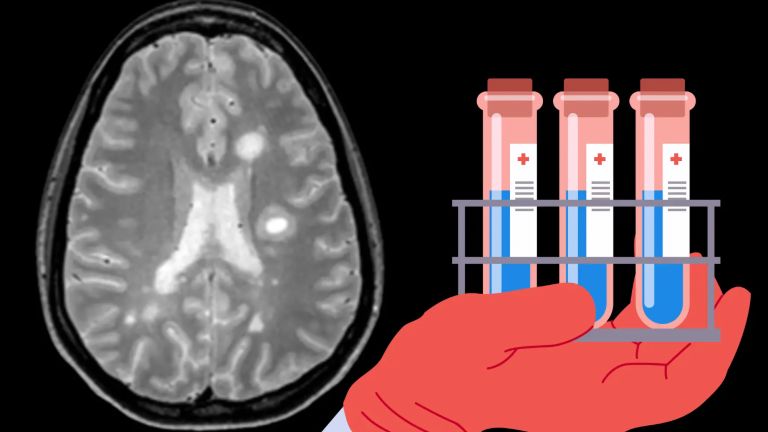
Der schubweise Verlauf von MS erschwerte bis vor wenigen Jahren die frühe Diagnose. Mittels Magnetresonanztomographie (MRT) sind die für MS typischen Entzündungsherde inzwischen aber bei mehr als 70 Prozent der Patienten schon in einem Stadium erkennbar, in dem es nur erste, unspezifische Symptome gibt.
Die so genannten McDonald-Kriterien zur Feststellung einer MS befinden sich aktuell in einer Aktualisierung, um eine frühere und genauere Diagnosestellung zu ermöglichen. Die erste Präsentation fand 2024 statt, die Publikation der finalen Kriterien steht noch aus. So kann zum Beispiel der Nachweis charakteristischer Muster (oligoklonale Banden) und Biomarker in der Rückenmarksflüssigkeit und die erweiterte Einbeziehung von Entzündungsherden unterschiedlichen Alters und mit einer spezifischen Verteilung den Ärzten zu einem schnelleren Urteil verhelfen. Bereits mit dem vorletzten Update 2017 war es gelungen, die Zeit bis zur Diagnosestellung von durchschnittlich 7,4 Monaten (nach den Kriterien von 2010) auf etwa 2,3 Monate zu verkürzen.
Mittels Bildgebung werden mitunter bei völlig symptomlosen Patienten Schäden im Gehirn entdeckt, die auf eine entzündliche Erkrankung des ZNS hinweisen. Dieses so genannte „radiologisch isolierte Syndrom“ verrät, dass zeitnah ein erster klinischer Schub zu erwarten ist. Bei einigen dieser Patienten würde der Nachweis spezifischer MRT-Merkmale oder Biomarker nach den vorgeschlagenen McDonald Kriterien 2024 eine sichere Diagnose und damit auch einen früheren Behandlungsbeginn erlauben.
Magnetresonanztomographie
Magnetresonanztomographie/-/magnetic resonance imaging
Ein bildgebendes Verfahren, das Mediziner zur Diagnose verschiedener Erkrankungen und Fehlbildungen in unterschiedlichen Geweben oder Organen des Körpers einsetzen. Die Methode wird umgangssprachlich auch Kernspin genannt. Sie beruht darauf, dass die Kerne mancher Atome einen Eigendrehimpuls besitzen, der sich im starken Magnetfeld ausrichtet. Diese Eigenschaft trifft unter anderem auf Wasserstoff zu. Deshalb können Gewebe, die viel Wasser enthalten, besonders gut dargestellt werden. Abkürzung: MRT.
Biomarker
Biomarker/-/biomarker
In der Medizin versteht man unter einem Biomarker eine Substanz, die Hinweise auf den physiologischen Zustand eines Organismus gibt. Biomarker können entweder im Körper selbst entstehen oder chemische Verbindungen beschreiben, die Ärzte dem Körper zuführen, um an ihrem Schicksal bestimmte physiologische Funktionen zu testen. In Bezug auf die Alzheimer-Krankheit sind mehrere Indikatoren als mögliche Biomarker im Gespräch. Hierbei handelt es sich beispielsweise um die Konzentration an löslichem Amyloid-Vorläuferprotein im Blut sowie um die Aktivität des Enzyms, welches das Vorläuferprotein so zerschneidet, dass hieraus das plaquebildende Beta-Amyloid hervorgeht. Oft werden auch krankheitsbezogene Veränderungen, die mit bildgebenden Verfahren nachgewiesen werden, als Biomarker bezeichnet. So kann man zum Beispiel den Abbau von Gehirngewebe im MRT erkennen.
Der französische Pathologe und Neurologe Jean-Martin Charcot (1825–1893) beschrieb als erster die Symptome: Seine „Charcot-Trias“ – Nystagmus (Augenzittern), Intentionstremor und abgehackte Sprache – galt lange als charakteristisch für die MS. Inzwischen weiß man, dass die Trias nur bei MS-Befall des Kleinhirns, also gar nicht so häufig, vorkommt, und darüber hinaus auch bei anderen Erkrankungen auftritt.
Augustus Frederick d’Este (1794–1848), ein Enkel des britischen Königs Georg III protokollierte in seinem Tagebuch als Erster den Verlauf der damals noch unbekannten Krankheit. Als erste Symptome traten bei d´Este mit 28 Jahren Sehstörungen auf, gefolgt von Schmerzen, Teillähmungen, und Sensibilitätsstörungen.
Multiple Sklerose
Multiple Sklerose/Encephalomyelitis disseminata/multiple sclerosis
Eine häufige neurologische Krankheit, die vorwiegend im jungen Erwachsenenalter auftritt. Aus noch ungeklärtem Grund greifen körpereigene Zellen die Myelinscheiden der Nervenzellen an und zerstören diese. Das kann im gesamten zentralen Nervensystem geschehen, weshalb zwei verschiedene Multiple-Sklerose-Patienten an ganz unterschiedlichen Symptomen leiden können. Häufige Beschwerden sind Sehstörungen, Taubheitsgefühle in Armen und Beinen, aber auch Koordinationsprobleme, Muskelschwäche und Blasenstörungen.
Rückenmark
Rückenmark/Medulla spinalis/spinal cord
Das Rückenmark ist der Teil des zentralen Nervensystems, das in der Wirbelsäule liegt. Es verfügt sowohl über die weiße Substanz der Nervenfasern, als auch über die graue Substanz der Zellkerne. Einfache Reflexe wie der Kniesehnenreflex werden bereits hier verarbeitet, da sensorische und motorische Neuronen direkt verschaltet sind. Das Rückenmark wird in Zervikal-, Thorakal-, Lumbal und Sakralmark unterteilt.
Geschädigte Axone als Basis der Symptome
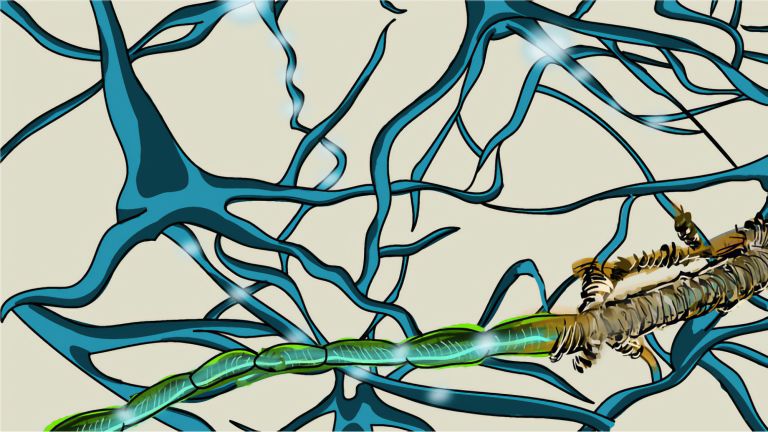
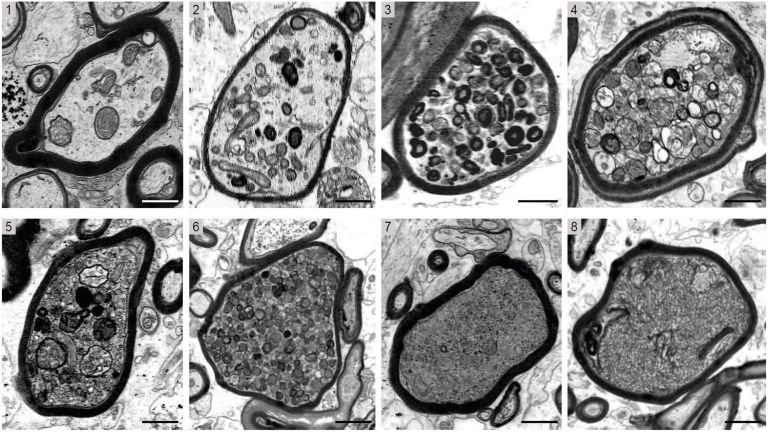
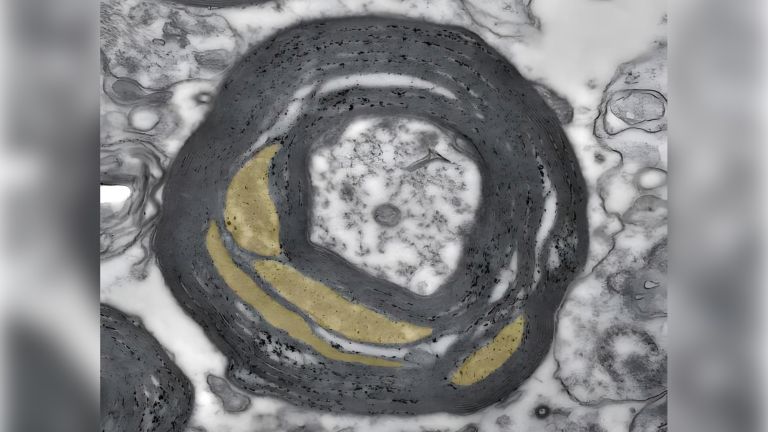
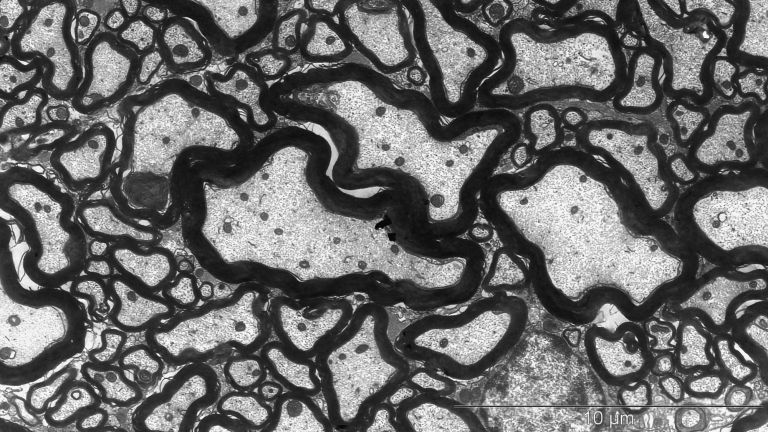
Bei der MS greift das Immunsystem die Isolierschicht der Axone an. Spezielle Gliazellen, die Oligodendrozyten, bilden in der grauen und weißen Substanz des Zentralen Nervensystems (ZNS) die Myelinscheiden der Axone, vergleichbar mit der Isolationsschicht eines Elektrokabels. Lücken zwischen den Myelinscheiden, die Ranvier’schen Schnürringe, ermöglichen hohe Leitungsgeschwindigkeiten bei der Übertragung von Nervenimpulsen, beim Menschen sind das bis zu 432 km/h. Zudem versorgen nach neueren Erkenntnissen die Oligodendrozyten die Axone mit wichtigen Nährstoffen. Die durch MS aktivierten Immunzellen verursachen Entzündungen an dieser Myelinschicht. Klingt die akute Entzündung ab, bildet sich an der Stelle faseriges Narbengewebe – diese Narben stören dann ebenfalls die Informationsübertragung. Bei fortgeschrittenen Krankheitsverläufen können später auch die Nerven selber (die Axone) geschädigt werden.
Im Prinzip können in allen Bereichen des ZNS Entzündungen auftreten. Betroffen sind aber vor allem die Sehnerven, das Rückenmark, der Hirnstamm und das Marklager um die Ventrikel. Auch in den Polen der Ventrikel und im Rückenmark entstehen gehäuft Entzündungsherde. Dabei gibt es einen engen Zusammenhang zwischen dem Ort der Schäden und den auftretenden Symptomen (siehe Kasten).
Etwa 85 Prozent der MS-Patienten leiden unter dem schubförmig remittierenden Verlauf der MS. Hier kommt es in der frühen Krankheitsphase zu einer Remyelinisierung: Die Myelinscheiden werden zwar wiederaufgebaut, die neurologischen Ausfälle bilden sich wieder vollständig zurück, die Weiterleitung der Impulse wird kompensiert. Allerdings bleiben die Myelinscheiden dünner. Mit zunehmender Erkrankungsdauer und abhängig von der Krankheitsaktivität erfolgt auch der Wiederaufbau nur noch teilweise, was zu bleibenden Behinderungen führt.
Oligodendrozyten
Oligodendrozyten/-/oligodendrocytes
Zellen des Zentralen Nervensystems, die die Myelinscheide um die Nervenzellen bilden und so deren Leitungsgeschwindigkeit erhöhen. Sie gehören zu den Gliazellen.
Hirnstamm
Hirnstamm/Truncus cerebri/brainstem
Der „Stamm“ des Gehirns, an dem alle anderen Gehirnstrukturen sozusagen „aufgehängt“ sind. Er umfasst – von unten nach oben – die Medulla oblongata, die Pons und das Mesencephalon. Nach unten geht er in das Rückenmark über. Er ist ein Zentrum lebenswichtiger Funktionen wie der Atmung und des Herzschlags und beinhaltet auf- und absteigende Bahnen zwischen Großhirn, Kleinhirn und Rückenmark.
Rückenmark
Rückenmark/Medulla spinalis/spinal cord
Das Rückenmark ist der Teil des zentralen Nervensystems, das in der Wirbelsäule liegt. Es verfügt sowohl über die weiße Substanz der Nervenfasern, als auch über die graue Substanz der Zellkerne. Einfache Reflexe wie der Kniesehnenreflex werden bereits hier verarbeitet, da sensorische und motorische Neuronen direkt verschaltet sind. Das Rückenmark wird in Zervikal-, Thorakal-, Lumbal und Sakralmark unterteilt.
Empfohlene Artikel
Oligodendrozyten als Tankstellen der Daten-Autobahnen
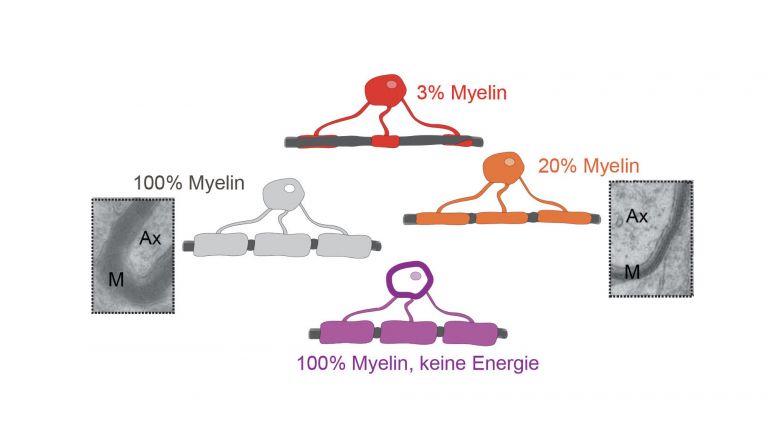
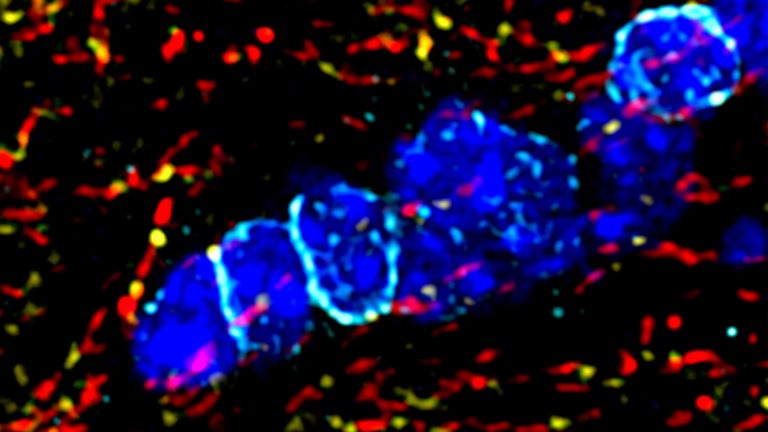
Zwar bilden die Oligodendrozyten zunächst neue Myelinscheiden, im Laufe der Krankheit gelingt ihnen das aber immer schlechter. Neben den Myelinscheiden können nämlich auch die Oligodendrozyten selbst von den Immunzellen angegriffen und zerstört werden. Oligodendrozyten spielen für die Bildung und Aufrechterhaltung einer intakten Myelinhülle eine Schlüsselrolle, sie sind für die „Wartungsarbeiten“ des Myelins verantwortlich. Doch die Isolierung der Axone ist nicht ihre einzige Aufgabe: Evolutionär noch älter ist die Versorgung der Axone. Klaus-Armin Nave, Direktor der Abteilung Neurogenetik am Max-Planck-Institut für Multidisziplinäre Naturwissenschaften in Göttingen, nennt Oligodendrozyten aufgrund ihrer Versorgungsfunktion für das Axon die „Tankstellen der Daten-Autobahnen“ des Nervensystems.
Die Fähigkeit zur Myelinbildung nimmt mit dem Alter deutlich ab. Damit verläuft die Behinderungsakkumulation stark altersabhängig. Beschädigte Axone werden nicht mehr elektrisch isoliert und mit Nährstoffen versorgt, in der Folge sterben nicht nur sie, sondern auch ihre Nervenzellen ab. Diffuse Läsionen der weißen Substanz und ein Rückgang an Hirnmasse und -volumen sind die Folge.
Eine Erklärung liefern Studien, die auf spezifische altersbedingte Veränderungen von Histonen hinweisen. Das sind Eiweiße, die eine wichtige Rolle bei der Verpackung der Erbsubstanz im Zellkern spielen. Durch an die Histone angehängte chemische Signale (Acetylgruppen) wird die „Verpackung“ an bestimmten Stellen gelockert. Dies scheint zu verhindern, dass sich aus den Vorläuferzellen der Oligodendrozyten reife, myelinbildende Oligodendrozyten entwickeln.
Zur Erforschung des Krankheitsgeschehens und zur Erprobung neuer Therapieansätze nutzen Forscher häufig das Modell der experimentellen Autoimmunenzephalitis (EAE). Dabei werden Versuchstiere gegen körpereigene Myelinbestandteile geimpft. Das hat zur Folge, dass sich das Immunsystem gegen Myelin und Oligodendrozyten richtet und so die Myelinscheiden zerstört werden. Auch isolierte autoreaktive T-Lymphozyten von solchermaßen erkrankten Tieren können die Krankheitserscheinungen hervorrufen, wenn sie gesunden Tieren übertragen werden.
Nach Einschätzung von Nave ist die Fokussierung auf das EAE-Modell zu einseitig. Zwar hat es Ähnlichkeit mit der MS, denn auch dort finden sich Zellen, die gegen körpereigene Myelinbestandteile gerichtet sind. Die Frage sei aber, was Henne und was Ei ist. Andere Modelle sind genauso wichtig für das Verständnis. Modelle etwa, bei denen primär neurodegenerative Veränderungen im Axon oder der Gliazelle zu einer sekundären Entzündung führen können. Denn auch diese aktiviert T-Zellen, die dann wiederum Schaden anrichten können.
Parallel zur Erforschung der grundlegenden Krankheitsmechanismen wurden in letzten Jahrzehnten große Fortschritte in der Therapie der MS erzielt. Noch ist sie zwar die häufigste Ursache neurologischer Behinderung bei jüngeren Erwachsenen, doch lässt sich der Verlauf bei den meisten Patienten verlangsamen und das Auftreten von Behinderungen verzögern, manchmal sogar ganz vermeiden. Auch die durchschnittliche Lebenserwartung hat deutlich zugenommen und nähert sich inzwischen der Allgemeinbevölkerung.
Oligodendrozyten
Oligodendrozyten/-/oligodendrocytes
Zellen des Zentralen Nervensystems, die die Myelinscheide um die Nervenzellen bilden und so deren Leitungsgeschwindigkeit erhöhen. Sie gehören zu den Gliazellen.
Axon
Axon/-/axon
Das Axon ist der Fortsatz der Nervenzelle, der für die Weiterleitung eines Nervenimpulses zur nächsten Zelle zuständig ist. Ein Axon kann sich vielfach verzweigen, und so eine Vielzahl nachgeschalteter Nervenzellen erreichen. Seine Länge kann mehr als einen Meter betragen. Das Axon endet in einer oder mehreren Synapse(n).
Myelin
Myelin/-/myelin
Myelin ist eine fetthaltige Substanz, die aus Gliazellen gebildet wird. Sie umhüllt die Axone (lange faserartige Fortsätze) von Nervenzellen und isoliert diese, so dass Nachrichten nicht unkontrolliert auf benachbarte Nervenzellen übergehen können. Zudem wird so die Signalleitung enorm beschleunigt.
Medizinische Möglichkeiten bei schubförmigem und progredientem Verlauf
Für den schubförmigen Verlauf stehen effektive Therapeutika zur Verfügung. Als Basistherapien gibt es seit langem die injizierbaren Beta-Interferone (Interferon-beta-1a und Interferon-beta-1b) und das Glatirameracetat. Hinzu kamen in den vergangenen Jahren Dimethylfumarat, Diroximelfumarat und Teriflunomid. Sie vermindern die Zahl der Entzündungsherde im Gehirn und reduzieren die Zahl der Schübe um 30 bis 50 Prozent im Vergleich zu Placebo.
Bei unzureichender Wirkung, oder wenn die MS von Beginn an einen aggressiven Verlauf nimmt, stehen mittlerweile ein halbes Dutzend Wirkstoffe zur Verfügung: Die S1P-Modulatoren Fingolimod, Ponesimod und Ozanimod; Natalizumab, Ocrelizumab, Ofatumumab / Ublituximab, Cladribin und als Reservemedikament bei Versagen der übrigen Therapieoptionen Alemtuzumab. Diese erreichen 50–80 % Schubreduktion, bergen aber teils höhere Risiken.
Bei jenen etwa 15 Prozent aller Patienten mit einer primär progredienten MS (PPMS) nehmen die Symptome von Krankheitsbeginn an zu – entweder langsam kontinuierlich oder unregelmäßig, mit Phasen zeitweiser Stabilisierung oder sogar vorübergehender geringer Besserung. Beim sekundär progredienten Verlauf geht die Erkrankung nach anfangs schubförmigem Verlauf in ein kontinuierliches Fortschreiten über. Ein schubförmiger Verlauf kann jederzeit in einen sekundär progredienten übergehen; manchmal schon bald nach dem ersten Auftreten der Erkrankung, manchmal erst nach mehreren Schüben. Bei beiden Formen ist die Therapie deutlich schwieriger als bei der schubförmigen MS.
Die einzige bisher zugelassene Therapie gegen die PPMS ist der Antikörper Ocrelizumab, der sich besonders bei jüngeren Patienten mit Entzündungsaktivität als wirksam erwiesen hat. Für aktive sekundär progrediente Krankheitsverläufe ist ebenfalls Ocrelizumab zugelassen, außerdem Siponimod.
Trotz vieler ungelöster Probleme sehen die meisten Ärzte und Wissenschaftler heute das Glas als halb voll an. Noch vor wenigen Jahrzehnten galt Multiple Sklerose als weitgehend unbehandelbar – heute stehen mehr als ein Dutzend zugelassene Therapien zur Verfügung, die den Krankheitsverlauf positiv beeinflussen können. Besonders ermutigend ist, dass auch in der progressiven MS zunehmend Fortschritte gemacht werden, etwa durch Antikörpertherapien, Remyelinisierungsansätze und neuroprotektive Strategien.
„Wir stehen nicht mehr am Anfang – wir sind mitten in einer Phase, in der wir Multiple Sklerose immer besser kontrollieren und vielleicht eines Tages sogar heilen können“, sagt Prof. Dr. Frauke Zipp, Neurologin an der Universitätsmedizin Mainz und Mitglied der Nationalen Akademie der Wissenschaften Leopoldina. „Was vor 15 Jahren noch unmöglich schien, ist heute Realität: Patientinnen und Patienten können mit MS ein fast normales Leben führen.“
Multiple Sklerose
Multiple Sklerose/Encephalomyelitis disseminata/multiple sclerosis
Eine häufige neurologische Krankheit, die vorwiegend im jungen Erwachsenenalter auftritt. Aus noch ungeklärtem Grund greifen körpereigene Zellen die Myelinscheiden der Nervenzellen an und zerstören diese. Das kann im gesamten zentralen Nervensystem geschehen, weshalb zwei verschiedene Multiple-Sklerose-Patienten an ganz unterschiedlichen Symptomen leiden können. Häufige Beschwerden sind Sehstörungen, Taubheitsgefühle in Armen und Beinen, aber auch Koordinationsprobleme, Muskelschwäche und Blasenstörungen.
Erstveröffentlichung am 1. November 2017
Letzte Aktualisierung am 15. August 2025