„Ich bin überzeugt davon, dass es klappen wird“

Alzheimer ist eine Krankheit, sie ist molekular recht gut verstanden – und sie ist besiegbar. Daran glaubt der Biochemiker Christian Haass aus München. Der Leibniz-Preisträger hat selbst ein paar entscheidende Entdeckungen gemacht.
Veröffentlicht: 20.09.2013
Niveau: mittel
Christian Haass, Jahrgang 1960, ging nach Abschluss seines Biologie-Studiums mit einem Stipendium in die USA. Die Jahre als Postdoc im Labor des Neurologen Dennis Selkoe an der Harvard-Universität waren prägend für ihn. Haass machte dort wichtige Entdeckungen zur Entstehung der Alzheimer-Krankheit. Zurück in Deutschland, forschte er ab 1995 zunächst am Zentralinstitut für Seelische Gesundheit in Mannheim, ab 1999 am Adolf-Butenandt-Institut der Ludwig-Maximilians-Universität München. Zusammen mit der Hans und Ilse Breuer Stiftung, deren Kuratorium er angehört, veranstaltet er jährlich eine wichtige Alzheimer-Fachkonferenz, das Eibsee Meeting. Außerdem ist er Standortsprecher des Deutschen Zentrums für Neurodegenerative Erkrankungen (DZNE) München.
Alois Alzheimer ist schon fast hundert Jahre tot. Wo steht die Forschung heute?
Christian Haass: Tja, wenn man der Presse folgt, steht die Forschung nicht gerade gut da. Da kann man zum Beispiel auf der ersten Seite der Süddeutschen in grünen Buchstaben lesen: „Das Scheitern der Alzheimer-Forschung“. Ich halte das allerdings für den größten Unsinn aller Zeiten. Ich glaube, dass gerade die Alzheimer-Forschung ein Paradebeispiel ist für gelungene moderne biomedizinische Forschung. Es ist eines der Arbeitsgebiete, die am besten und am erfolgreichsten erforscht worden sind in der gesamten Biomedizin.
Ein erstaunlicher Unterschied in der Bewertung!
Ich war ziemlich sauer und habe mit der Süddeutschen einen Riesenkrach gekriegt deswegen. Weil es politisch enorm schädlich ist, was die behauptet haben, weil es den Patienten schadet und der Wissenschaft auch.
Gab es einen Anlass für diese negative Einschätzung?
Ja, einen ganz einfachen Anlass. Es gab eine Pressemitteilung, dass mal wieder eine klinische Studie nicht funktioniert hat. Es ging um ein Medikament, das sich gegen das Beta-Amyloid richtet, an dem wir ebenfalls forschen, und es war schon die dritte oder vierte Studie, die nicht geklappt hatte. Und die Journalistin schloss daraus: Wenn das alles nicht funktioniert, ist das Amyloid nicht die Ursache. Ihr arbeitet alle am falschen Zielmolekül. Sie hatte allerdings nur Leute interviewt, die keine Ahnung von moderner Forschung haben. Und mit mir wollte sie nicht reden. Dabei sieht das Bild, realistisch betrachtet, völlig anders aus!
Würden Sie denn sagen, dass der Mechanismus der Alzheimer-Krankheit im Prinzip verstanden ist?
Teilweise ja. Es stimmt einfach nicht, dass wir nichts über Alzheimer wissen. Wir wissen sehr gut, wie die Krankheit ausgelöst wird. Wir wissen auch sehr gut, wie man sie verhindern kann. Das Problem ist, dass die Patienten, wenn sie in die Klinik kommen, die Krankheit schon haben. Das ist zu spät. Wir müssen prophylaktisch arbeiten.
Können Sie kurz beschreiben, wie Alzheimer entsteht?
Ich bin ein großer Anhänger der Amyloid-Theorie. Alois Alzheimer hat ja bereits herausgefunden, dass im Gehirn von Patienten eine Art Klumpen entstehen, Protein-Ablagerungen. Und eine Art dieser auffälligen Ablagerungen sind die so genannten Plaques. Die bestehen aus dem Amyloid-beta-Peptid. Und dieses Peptid, ein kleines Protein, entsteht ganz normal in unserem Gehirn, allerdings muss es herausgeschnitten werden aus einem größeren Vorläuferprotein, dem APP. Man hat ursprünglich gedacht, das passiert nur bei Patienten, weil nur sie diese Plaques haben. Ich habe aber 1992 in den USA herausbekommen, dass es bei uns allen passiert – auch schon in jungen Jahren. Ich habe das zu meinem Erschrecken bei mir selbst festgestellt. In meinem eigenen Blut habe ich das Amyloid gefunden …
Wirklich?
Ja, das war schon etwas erschreckend. Aber ich habe es bei meinem Chef genauso gefunden, der hat noch mehr im Blut gehabt – und das als Harvard-Professor! Wir haben dann gefunden, dass jede Zelle Amyloid macht und dass das ganz normal ist. Vor allem bei Nervenzellen. Und diese Entdeckung hatte zur Folge, dass man konzeptionell völlig umdenken musste: Wir alle haben ein hohes Risiko. Zum anderen hat sie die Forschung massiv angestoßen.
Inwiefern?
Weil man damit ein einfaches System hatte, mit dem man den Mechanismus der Amyloid-Entstehung sehr gut erarbeiten konnte. Man konnte die Enzyme identifizieren, die das Peptid aus dem APP herausschneiden, die Sekretasen. Man konnte in Reihenuntersuchungen Wirkstoffe finden, die die Amyloidproduktion blockieren. Die Wirkstoffe, die heute in der Klinik sind und gegen die Sekretasen wirken, sind alle mit dem Zellkultursystem von damals gefunden worden.
Warum gibt es dann Zweifel an der Amyloid-Theorie?
Viele Leute behaupten: Amyloid ist nicht die Ursache, denn es korreliert nicht mit der Demenz. Da gibt es eine berühmte Studie an Nonnen. Es waren Nonnen gestorben, die geistig völlig fit waren, und nach ihrem Tod fand man ihr Gehirn voller Plaques.
Plaques
senile Plaques/-/senile plaques
Senile Plaques lagern sich in der grauen Hirnsubstanz ab, wenn ein Eiweiß – das so genannte Amyloid-Vorläuferprotein – nicht korrekt abgebaut wird. Entzündungen sowie Erkrankungen des Fett– oder des Zuckerstoffwechsels können die Plaquebildung begünstigen. Im Schnitt erreichen die Ablagerungen einen Durchmesser von 50 Mikrometern. Das Auftreten von Plaques ist eine von mehreren anatomischen Veränderungen im Gehirn, anhand derer Pathologen nach dem Tod eine Alzheimer-Erkrankung diagnostizieren können.
Sekretasen
Sekretasen/-/secretases
Sekretasen sind Proteasen, die Proteine in kleinere Fragmente spalten, oft membranständig bei Transmembranproteinen. Durch die Spaltung entstehen intrazelluläre Fragmente, die als Signal wirken können, und extrazelluläre Fragmente, die in die Umgebung freigesetzt werden. Manche Proteine, wie das Amyloid-Vorläuferprotein (APP), bieten verschiedenen Sekretasen unterschiedliche Schnittstellen. Beta-Amyloid, der Hauptbestandteil seniler Plaques, entsteht, wenn APP zunächst von der β-Sekretase außerhalb der Membran und anschließend von der γ-Sekretase innerhalb der Membran geschnitten wird.
Demenz
Demenz/Dementia/dementia
Demenz ist ein erworbenes Defizit kognitiver, aber auch sozialer, motorischer und emotionaler Fähigkeiten. Die bekannteste Form ist Alzheimer. „De mentia“ bedeutet auf Deutsch „ohne Geist“.
Wie kann man diese Widersprüche auflösen? Kann man das überhaupt?
Ja. Die Natur hat die Frage auf die einfachste Weise spektakulär beantwortet. Wir selbst haben 1993 noch gefunden, dass eine Mutation, die auf genetisch vererbtem Weg zu Alzheimer führt, genau an der Stelle wirkt, wo die eine der beiden Sekretasen schneiden muss, um das Amyloid freizusetzen. Die Mutation verändert das Amyloid so, dass die Sekretase leichter schneiden kann – es entsteht also mehr Amyloid. Diese Patienten produzieren also mehr Amyloid und bekommen die Krankheit deutlich früher. 2012 wurde eine ähnliche Entdeckung gemacht. Nur hatte man umgedacht: Man hat nicht Patienten gesucht, die früher Alzheimer kriegen, sondern man hat nach Menschen gesucht, die im hohen Alter vor Alzheimer geschützt sind. Ein extrem schlauer Ansatz, den wir schon lange gefordert hatten.
Wieso erst jetzt?
Es ging eigentlich nur mittels einer sehr großen Studie, die man in Island gemacht hat. Island ist populationsgenetisch schon immer etwas abgeschlossen, sehr klein, und in Island wurde das Genom vieler Einwohner sequenziert. So hat man eine Genveränderung gefunden, die vor Alzheimer schützt. Und der Hammer war: Diese Genveränderung sitzt genau an der Stelle, wo die Alzheimer-Mutation sitzt. Und sie verändert das Vorläufer-Protein APP in einer Weise, dass die Sekretase nicht mehr schneiden kann.
Also ein klarer Dosis-Effekt?
Genau. Mehr Amyloid: Man bekommt die Krankheit. Weniger Amyloid: Man ist geschützt. Die Natur zeigt uns also, dass Amyloid die Ursache ist. Und die Natur hat bereits das Experiment durchgeführt, das beweist, dass eine Amyloid-Erniedrigung uns vor der Krankheit schützt. Es war übrigens dieselbe Mutation, die wir 1994 künstlich hergestellt und in Zellkultur getestet hatten. Ein klarer Beweis, ich war total begeistert!
Aber welche Rolle spielt dann das andere Protein, das bei Alzheimer auffällig erhöht ist, das Tau?
Das spielt auch eine extrem wichtige Rolle! Ich denke, es ist eine Kaskade: Das Amyloid wirkt von außen ganz oben in der Kaskade der Ursachen, unten wirkt das Tau innerhalb der Zelle. Wir müssen dabei auch im Kopf behalten, dass es eine andere Demenzerkrankung gibt, die Frontotemporale Demenz, da haben viele Betroffene nur Tau-Ablagerungen, keine Plaques. Offensichtlich ist das Tau-Protein der Vollstrecker, der die Zellen umbringt. Und das Amyloid stupst das Ganze an.
Es werden ja noch andere Faktoren diskutiert: Es könnte an den Mitochondrien liegen. Es könnte an Entzündungen liegen. Es könnte an Umweltfaktoren wie Kupfer liegen. Sind diese Faktoren nebensächlich?
Entzündungen halte ich für enorm wichtig. Das ist bisher zu wenig erforscht worden. Ein weiterer Faktor ist die vaskuläre Dysfunktion: Alle Alzheimer-Patienten zeigen im Gehirn Ablagerungen des Amyloids im Blutgefäßsystem und damit verbunden Blutungen. Und es gibt meines Wissens keinen einzigen Alzheimerfall, bei dem nicht auch eine Entzündung vorliegt. Diese Punkte werden oft separat bearbeitet und nicht zusammengebracht. Deswegen haben wir hier in München unser Exzellenzcluster, das Munich Cluster for Systems Neurology, kurz SyNergy, so aufgebaut, dass wir an der Schnittstelle von vaskulärer Dysfunktion, Neuroinflammation und Neurodegeneration arbeiten. Wir versuchen, die Spezialisten gezielt zusammenzubringen, um gemeinsam Fortschritte zu machen.
Sekretasen
Sekretasen/-/secretases
Sekretasen sind Proteasen, die Proteine in kleinere Fragmente spalten, oft membranständig bei Transmembranproteinen. Durch die Spaltung entstehen intrazelluläre Fragmente, die als Signal wirken können, und extrazelluläre Fragmente, die in die Umgebung freigesetzt werden. Manche Proteine, wie das Amyloid-Vorläuferprotein (APP), bieten verschiedenen Sekretasen unterschiedliche Schnittstellen. Beta-Amyloid, der Hauptbestandteil seniler Plaques, entsteht, wenn APP zunächst von der β-Sekretase außerhalb der Membran und anschließend von der γ-Sekretase innerhalb der Membran geschnitten wird.
Hammer
Hammer/Maleus/hammer
Der erste der kleinen Gehörknöchelchen im Mittelohr. Er ist mit dem Trommelfell verbunden und überträgt die durch die Schallwellen ausgelöste Vibration über die beiden anderen Gehörknöchelchen (Amboss, Steigbügel) zur Gehörschnecke, wo der Reiz in ein neuronales Signal umgewandelt wird.
Plaques
senile Plaques/-/senile plaques
Senile Plaques lagern sich in der grauen Hirnsubstanz ab, wenn ein Eiweiß – das so genannte Amyloid-Vorläuferprotein – nicht korrekt abgebaut wird. Entzündungen sowie Erkrankungen des Fett– oder des Zuckerstoffwechsels können die Plaquebildung begünstigen. Im Schnitt erreichen die Ablagerungen einen Durchmesser von 50 Mikrometern. Das Auftreten von Plaques ist eine von mehreren anatomischen Veränderungen im Gehirn, anhand derer Pathologen nach dem Tod eine Alzheimer-Erkrankung diagnostizieren können.
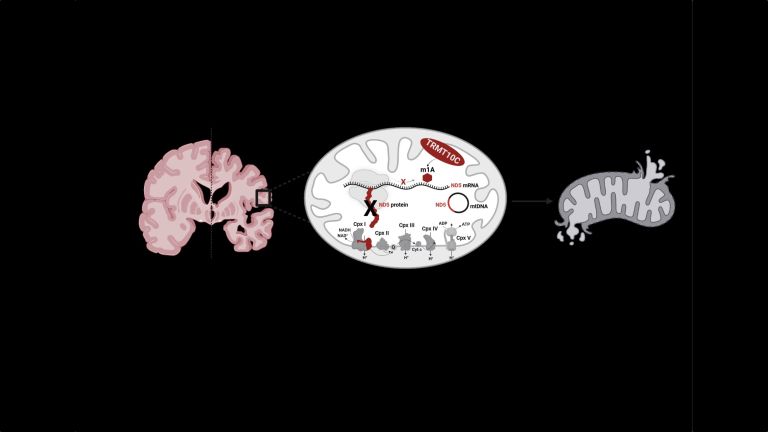
Mitochondrien
Mitochondrien/-/mitochondria
Mitochondrien sind Organellen im Inneren einer Zelle, sie werden auch als „Kraftwerk“ der Zellen bezeichnet, da sie diese mit Energie versorgen. Sie haben eine eigene DNA, die nur über die Mutter vererbt wird.
Neurodegeneration
Neurodegeneration/-/neurodegeneration
Sammelbegriff für Krankheiten, in deren Verlauf Nervenzellen sukzessive ihre Struktur oder Funktion verlieren, bis sie teilweise sogar daran zugrunde gehen. Vielfach sind falsch gefaltete Proteine der Auslöser – wie etwa bestimmte Formen der Eiweiße Beta-Amyloid und Tau im Falle von Alzheimer. Bei anderen Krankheiten, beispielsweise bei Parkinson oder Chorea Huntington, werden Proteine innerhalb der Neurone nicht richtig abgebaut. In der Folge lagern sich dort toxische Aggregate ab, was zu den jeweiligen Krankheitserscheinungen führt. Während Chorea Huntington eindeutig genetisch bedingt ist, scheint es bei Parkinson und Alzheimer allenfalls bestimmte Ausprägungsformen von Genen zu geben, welche ihre Entstehung begünstigen. Keine dieser neurodegenerativen Erkrankungen kann bisher geheilt werden.
Empfohlene Artikel
Man hört aber auch die Meinung, Alzheimer sei gar keine Krankheit. Es sei so verbreitet, es sei Teil des gewöhnlichen Alterns. Wie stehen Sie dazu?
Naja, basierend auf meiner eigenen Forschung müsste ich ja sagen: Das ist so. Andererseits – es kriegt ja nicht jeder Alzheimer. Wir haben bereits über die Isländer gesprochen, die durch eine Mutation geschützt sind. Also, das ist schon ein Krankheitsprozess, der bei manchen Leuten früher abläuft und bei anderen später. Das frühere Ablaufen ist auf jeden Fall krankhaft – offensichtlich wird das Amyloid nicht richtig abgeräumt. Andererseits muss man natürlich sehen: Jeder von uns produziert das Amyloid. Den Grundstein legen wir alle permanent. Wir müssen im Alter damit leben.
Wenn Alzheimer eine Krankheit ist, müsste sie auch heilbar sein. Die bisherigen Medikamente leisten das nicht, weil sie nicht an der Ursache ansetzen. Wie müsste denn ein Medikament aussehen, das Alzheimer heilt?
Der beste Ansatz ist meiner Meinung nach momentan die Impfung. Rechtzeitig angewandt, müsste sie Alzheimer verhindern.
Und warum haben wir die noch nicht?
Weil man bisher Menschen geimpft hat, die Alzheimer bereits hatten. Bei denen wurden nach der Impfung die Plaques im Gehirn abgeräumt, das wissen wir bereits. Das zeigt eigentlich, dass der Ansatz korrekt ist: Man trifft das Zielmolekül und wird es los. Das Problem ist, dass die Neurodegeneration schon da war, bevor man mit der Impfung begonnen hat. Das Ganze muss also erheblich früher stattfinden. Dafür gibt es jetzt einen Ansatz mit der weltweiten DIAN-Studie: Dabei werden genetisch vererbte Alzheimer-Fälle registriert, biologische Proben genommen wie Blut und Gehirnflüssigkeit, und die Betroffenen werden einbezogen in klinische Studien. Die Zielrichtung ist dabei klar: Man möchte Leute haben, die von ihrer Veranlagung her die Krankheit hundertprozentig bekommen, diese aber, bevor sie die Symptome zeigen – und damit verbunden neuronalen Zellverlust –, in die Studie einschleusen. Die ersten Impfungen in der DIAN-Studie haben 2013 stattgefunden, es gibt also noch keine Ergebnisse.
Warum sind wir bei der Behandlung noch nicht weiter? Tut die Pharma-Industrie nicht genug?
Im Moment steigen viele Pharma-Firmen aus, es ist eine Katastrophe. Denn die klinischen Studien sind extrem teuer, und oft funktionieren sie nicht. Unverständlich ist mir aber auch, dass die Firma Eli Lilly einen Gamma-Sekretase-Inhibitor in die Klinik bringen konnte, von dem man vorhersagen konnte, dass er katastrophale Wirkungen haben wird. Die haben diesen Wirkstoff an Patienten angewandt – entgegen allen wissenschaftlichen Daten, auch aus meinem Labor. Wir konnten denen ziemlich exakt vorhersagen, was im Menschen passieren wird. Und genau das ist auch passiert: Die Patienten bekamen Hauttumoren, Magen-Darm-Probleme, und das Gedächtnis wurde noch schlechter, weil es den Menschen immer schlechter ging. Die Studie musste abgebrochen werden. Im Juli 2013 ist dann im New England Journal of Medicine eine Untersuchung erschienen, die impliziert, dass es vielleicht sogar dosisabhängig Tote gab.
Ein grausamer Menschenversuch!
So etwas darf nicht passieren. Auf der anderen Seite sehe ich ein riesiges gesellschaftliches Problem: Die Krankheit wird immer häufiger werden, und die Industrie wird immer mehr aus der Forschung aussteigen. Es ist jetzt schon so, dass wir Wissenschaftler, auch im Deutschen Zentrum für Neurodegenerative Erkrankungen, immer öfter von Politikern aufgefordert werden, doch endlich Medikamente zu liefern. Das können wir aber gar nicht, das ist nicht unsere Aufgabe. Das ist viel zu teuer. Die machen sich keine Vorstellung, was das kostet.
Was also müsste geschehen?
Es ist auch für eine einzelne Firma zu teuer. Deswegen glaube ich – und das mag total blauäugig sein – dass wir ein Riesenkonsortium brauchen aus vielen großen Firmen plus vielen großen Staaten, die das Ganze gemeinsam finanzieren. Das ist eine Aufgabe, an der nicht eine Firma reich werden darf. Das ist eine Aufgabe, die die gesamte Menschheit betrifft. Das ist ähnlich wie beim Umweltschutz. Das sind Fragen, die uns alle betreffen. Und die eilig sind. Es muss extrem viel Geld auf den Tisch, und es muss international gearbeitet werden.
Gesetzt den Fall, das würde klappen: Haben Sie Hoffnungen, dass Alzheimer bald kein Problem mehr sein wird?
Bald würde ich nicht sagen. Und ich werde mich auch nicht zeitlich festlegen. Aber die Hoffnung habe ich ganz klar: Nachdem man die Mechanismen doch recht gut im Griff hat und mehrere Ansätze für Medikamente, die sicherlich noch verbesserungswürdig sind … Ich bin überzeugt davon, dass es klappen wird! Wenn wir die Patienten früh genug behandeln können.
Plaques
senile Plaques/-/senile plaques
Senile Plaques lagern sich in der grauen Hirnsubstanz ab, wenn ein Eiweiß – das so genannte Amyloid-Vorläuferprotein – nicht korrekt abgebaut wird. Entzündungen sowie Erkrankungen des Fett– oder des Zuckerstoffwechsels können die Plaquebildung begünstigen. Im Schnitt erreichen die Ablagerungen einen Durchmesser von 50 Mikrometern. Das Auftreten von Plaques ist eine von mehreren anatomischen Veränderungen im Gehirn, anhand derer Pathologen nach dem Tod eine Alzheimer-Erkrankung diagnostizieren können.
Neurodegeneration
Neurodegeneration/-/neurodegeneration
Sammelbegriff für Krankheiten, in deren Verlauf Nervenzellen sukzessive ihre Struktur oder Funktion verlieren, bis sie teilweise sogar daran zugrunde gehen. Vielfach sind falsch gefaltete Proteine der Auslöser – wie etwa bestimmte Formen der Eiweiße Beta-Amyloid und Tau im Falle von Alzheimer. Bei anderen Krankheiten, beispielsweise bei Parkinson oder Chorea Huntington, werden Proteine innerhalb der Neurone nicht richtig abgebaut. In der Folge lagern sich dort toxische Aggregate ab, was zu den jeweiligen Krankheitserscheinungen führt. Während Chorea Huntington eindeutig genetisch bedingt ist, scheint es bei Parkinson und Alzheimer allenfalls bestimmte Ausprägungsformen von Genen zu geben, welche ihre Entstehung begünstigen. Keine dieser neurodegenerativen Erkrankungen kann bisher geheilt werden.
Gedächtnis
Gedächtnis/-/memory
Gedächtnis ist ein Oberbegriff für alle Arten von Informationsspeicherung im Organismus. Dazu gehören neben dem reinen Behalten auch die Aufnahme der Information, deren Ordnung und der Abruf.
zum Weiterlesen:
- Haass, C: Initiation and propagation of neurodegeneration, Nature Medicine 2010 Nov;16(11):1201 – 4 (zum Abstract).
- Haass, C: Alzheimer – Mechanismen und therapeutische Ansätze, Biologie in unserer Zeit 2009;39(2):92 – 100 (zum Abstract).
- Informationen zur DIAN-Studie, bei der die seltene Form der „dominant vererbten Alzheimer-Krankheit“ erforscht und Impfungen erprobt werden; URL: http://www.dian-info.org/de/ [Stand: 05.09.2013]; zur Webseite.
![Ein Protein, das in der Zellmembran sitzt, kann durch zwei molekulare Schnitte zu einem schädlichen Peptid verkürzt werden: dem Beta-Amyloid. Grafikerin: Meike Ufer [nach Haass 2010]](https://www.dasgehirn.info/sites/default/files/styles/scale_768_w/public/images/copy_of_4_8_3_Alzheimer_Ansicht.jpg?itok=d4Zm9kD9)