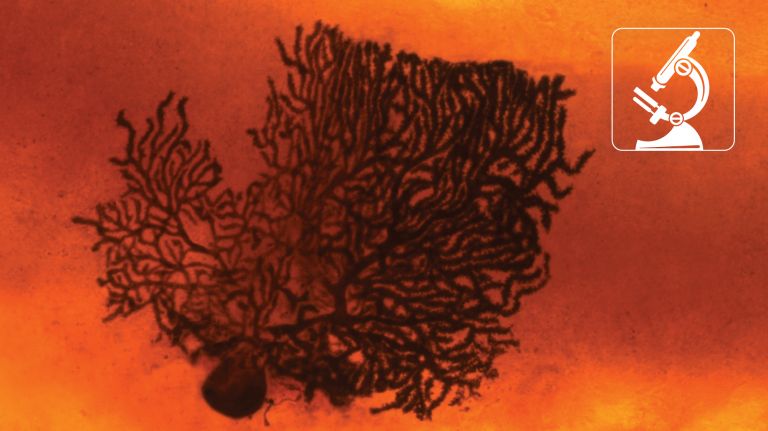
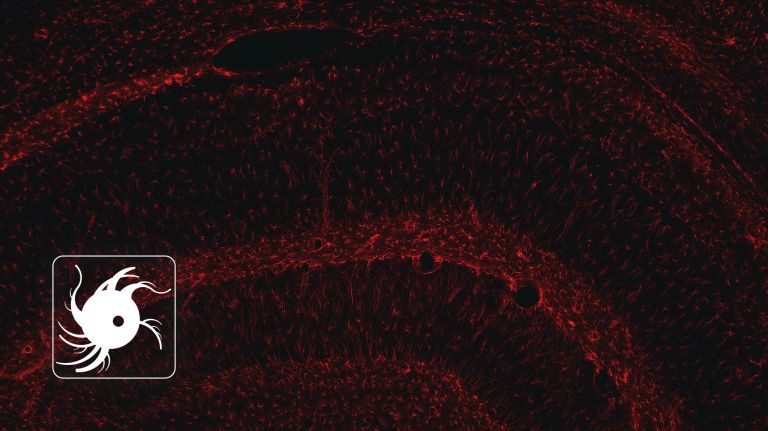
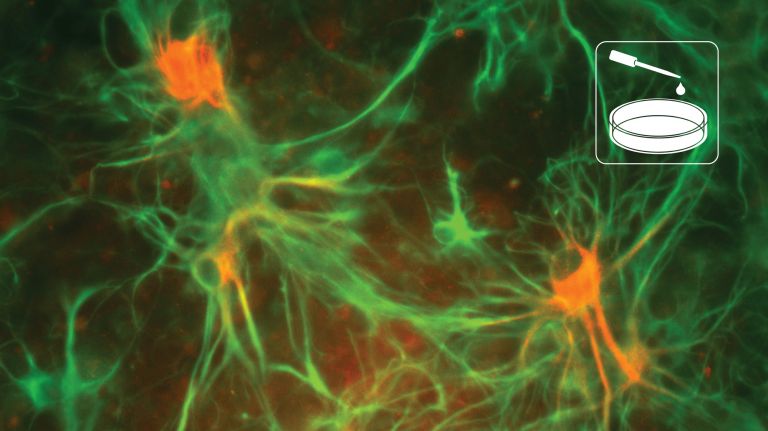
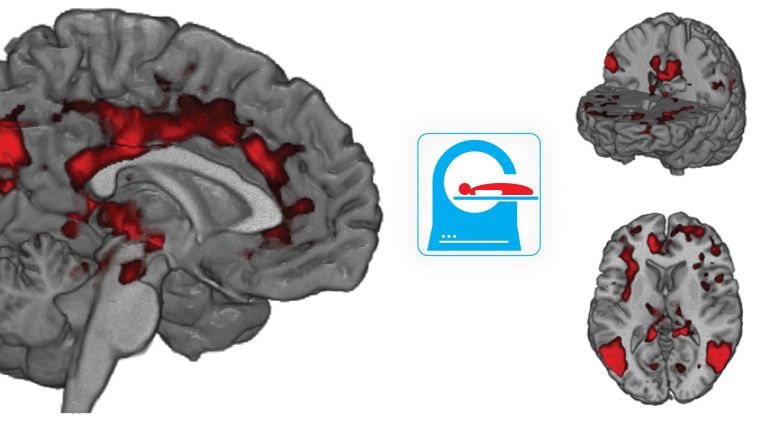
Mikroelektroden
Die Hirnforschung nutzt verschiedene wissenschaftliche Methoden. Hier stellen wir Ihnen zentrale Arbeitstechniken vor. Zum Beispiel die Elektrophysiologie mit Mikroelektroden.
Wissenschaftliche Betreuung: Prof. Dr. Alexander Gail
Veröffentlicht: 21.07.2016
Niveau: mittel
- Mikroelektroden sind elektrische Leiter, die den direkten Zugang zur Umgebung einzelner Zellen oder gar ihrem Inneren erlauben.
- Mit ihnen lässt sich die Aktivität einzelner Nervenzellen messen und wie diese sich nach natürlichen Reizen ändert, aber auch nach experimentellen Veränderungen an der Zelle oder ihrer Umgebung.
- Mikroelektroden wurden zuerst im frühen 20. Jahrhundert eingesetzt. Wichtige Entwicklungen gehen zurück auf Alan Hodgkin und Andrew Huxley sowie Bert Sakman und Erwin Neher.
- Die Methode kann einzelne Aktionspotenziale auflösen, die Basiseinheit der elektrischen Kommunikation von Nervenzellen. Sie ist allerdings auf nur wenige Zellen gleichzeitig anwendbar.
- Für eine räumliche Einordnung der Daten muss die elektrische Messung mit mikroskopischen Methoden kombiniert werden. Auch zur Kontrolle mancher gentechnischer Veränderungen lässt sie sich einsetzen.
- Eine aktuelle Entwicklung geht in Richtung so genannter Multielektrodenarrays, die elektrische Aktivität auf deutlich mehr Kanälen gleichzeitig messen können. Aber es gibt auch bereits Versuche, die Elektroden bei der elektrischen Messung ganz zu ersetzen.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
Aktionspotenzial
Aktionspotenzial/-/action potential
In erregbaren Zellen (z. B. Neuronen oder Muskelzellen) findet man sehr schnelle Änderungen des elektrischen Potenzials über der Zellmembran. Dieses Ereignis ist die Grundlage für die Informationsleitung entlang des Axons der Nervenzelle. Das Aktionspotenzial setzt sich entlang der Zellmembran fort und entsteht nach dem Alles-oder-Nichts-Prinzip nur dann, wenn die Zelle ausreichend stark erregt wurde.
Viele Sprachbilder über unser Gehirn mögen falsch sein. Aber der „Geistesblitz“ hat tatsächlich eine Entsprechung in unserem Kopf. Nervenzellen kommunizieren untereinander mit elektrischen Signalen. Diese zu messen, erlaubt die Elektrophysiologie mit Mikroelektroden.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
Funktionsweise
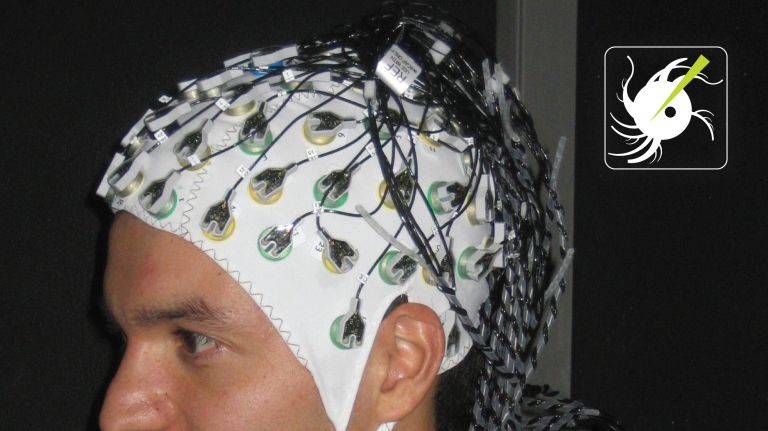
Es handelt sich dabei um haarfein ausgezogene Glaspipetten oder Metalldrähte, die in die Nervenzellen gestochen oder in die Nähe der Membran platziert werden. Im Gegensatz zu anderen Verfahren wie etwa der Elektroenzephalografie (EEG) oder der Kernspinresonanz (NMR) können Mikroelektroden also die Aktivität individueller Nervenzellen erfassen und bieten damit eine extrem hohe räumliche Auflösung des Geschehens im Gehirn.
Beim Menschen etwa sind die Nervenzellen in der Regel nur bis zu einhundert Mikrometer groß. Mit einem elektrischen Leiter muss man also erst einmal nah genug an eine einzelne Zelle herankommen, um Spannungsänderungen oder Stromfluss in ihr zu registrieren und an das Messgerät weiterzuleiten. Das Milieu, in dem Zellen überleben können, ist allerdings selbst elektrisch leitfähig. Steckte man einfach einen Draht hinein, würde der auf seiner ganzen Länge elektrische Ladungen mit seiner Umgebung austauschen.
Trotzdem gibt es Mikroelektroden aus feinen Metalldrähten. Sie werden nach außen mit verschiedenen nicht-leitenden Materialien isoliert. Mit ihnen lassen sich elektrische Vorgänge vor allem außerhalb der Zelle – „extrazellulär“ – messen.
Alternativ verwenden Forscher so genannte „Mikropipetten“. Sie bestehen außen aus einer feinen Glaskapillare, die unter genau kontrollierten Bedingungen erhitzt und auseinandergezogen wird. So entsteht eine enge Spitze von weniger als einem Mikrometer Durchmesser. Nur an dieser Stelle hat das Innere jetzt noch Kontakt mit dem umgebenden Medium. Füllt man die Kapillare mit einer leitfähigen Flüssigkeit, verrät der darin fließende Strom, was vor ihrer Spitze geschieht.
Konzentrierte Salzlösung zum Beispiel funktioniert als elektrischer Leiter, oft aber benutzen Forscher andere Lösungen, die noch stärker an das Milieu im Zellinneren angepasst sind. Die klassische so genannte intrazelluläre Messung bringt nämlich beide Lösungen in direkten Kontakt: Dabei wird die Spitze der Elektrode durch die Zellmembran gestochen, um elektrische Vorgänge im Inneren messen zu können. Nervenzellen können ihre Membran nach so einem Einstich erstaunlich gut wieder abdichten. Mehrere Stunden lang überleben sie und bleiben aktiv – allerdings nur, wenn ihr Inneres nicht durch den Inhalt der Mikropipette zu sehr verdünnt wird.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
EEG
Elektroencephalogramm/-/electroencephalography
Bei dem Elektroencephalogramm, kurz EEG handelt es sich um eine Aufzeichnung der elektrischen Aktivität des Gehirns (Hirnströme). Die Hirnströme werden an der Kopfoberfläche oder mittels implantierter Elektroden im Gehirn selbst gemessen. Die Zeitauflösung liegt im Millisekundenbereich, die räumliche Auflösung ist hingegen sehr schlecht. Entdecker der elektrischen Hirnwellen bzw. des EEG ist der Neurologe Hans Berger (1873−1941) aus Jena.
Einsatzgebiete
Mikroelektroden erlauben Hirnforschern wichtige Einblicke in die Details der Informationsverarbeitung im Gehirn. Mit ihnen lassen sich Aktionspotenziale, die Informationseinheiten einzelner Zellen, messen. Wie diese entstehen und welchen Einfluss verschiedenste Manipulationen auf sie und auch auf das Ruhepotenzial der Zelle haben, all das haben Wissenschaftler mit dieser Methode bereits weitgehend aufgeklärt.
Mit Mikroelektroden können die Forscher aber auch umgekehrt niedrig dosierte Ströme durch die Zelle schicken und deren Reaktion messen. Fast alles, was wir über die elektrische Aktivität der einzelnen Nervenzelle wissen Sprache der Neurone, beruht auf Messungen mit Mikroelektroden. So haben Forscher sehr viel über Reizstärken, die Bedeutung der Konzentration von Ionen in und um die Nervenzelle sowie die Aktivität von Kanal– und Transporter-Molekülen gelernt.
Kein Wunder, dass eine ganze Reihe von Nobelpreisen an Wissenschaftler vergeben wurden, die die Aufnahmetechniken mit Mikroelektroden begründet und verfeinert haben. Da nun viele Prozesse recht klar sind, reicht oft schon eine elektrische Messung, um auf Veränderungen der verschiedenen Komponenten zurückzuschließen – sei es nach Lernvorgängen oder nach genetischen Manipulationen.
Ruhepotenzial
Ruhepotenzial/-/steady-state potential
Das Membranpotenzial eines Neurons im Ruhezustand. Der Einstrom und Ausstrom von Ionen ist im Gleichgewicht. Es beträgt ca. –80mV.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
Historie
Auch wenn schon 1786 Luigi Galvani der erste war, der lebendes Gewebe mit Elektrizität in Berührung brachte: Ansätze, umgekehrt die natürliche elektrische Aktivität dieses Gewebes zu messen, benötigten feinere Messgeräte. Erste Versuche, etwa von Emil Du Bois-Reymond in den 1840er Jahren, nutzten Galvanometer, die den Stromfluss aus der Auslenkung einer Magnetnadel zurückrechneten. Mit dieser Methode ließ sich aber nur die Gesamtaktivität von ganzen Muskeln und Nervenbündeln erfassen.
Direkte Messungen mit Elektroden wurden erst im 20. Jahrhundert möglich. Alan Hodgkin und Andrew Huxley waren 1939 die ersten, die eine besonders feine Elektrode in das Innere einer Nervenzelle einführten. Die Riesenaxone von Tintenfischen machten es möglich: Mit einem Durchmesser von bis zu einem Millimeter sind sie hundert– bis tausendmal so dick wie die des Menschen. Aus ihren Daten berechneten die beiden späteren Nobelpreisträger ein mathematisches Modell des Aktionspotenzials, das heute noch gelehrt wird.
Einen weiteren Nobelpreis für die Fortentwicklung der Aufnahmetechniken erhielten 1991 Bert Sakmann und Erwin Neher. Sie hatten in den 1970er Jahren die Patch-Clamp-Methode entwickelt, mit der sich Ströme durch einzelne Ionenkanäle in einer Zellmembran messen lassen, im Bereich von 1 pA, einem Billionstel eines Ampere. Beim Patch-Clamping wird die Elektrode nicht mehr in die Zelle gestochen, sondern nur auf die Zellmembran aufgesetzt. Mit einem leichten Saugen lässt sich die Elektrode so gut mit der Zellmembran versiegeln, dass dazwischen so gut wie kein Strom mehr fließt. Alle Ladungsträger, die sich durch das winzige Stück Membran direkt unter der Glaskapillare bewegen, werden jetzt von dieser registriert. Im Extremfall eines einzelnen Ionenkanals werden so noch Ströme im Bereich von einem Billionstel Ampere erfasst.
Eine relativ neue Entwicklung sind die Multielektrodenarrays. Sie vereinen auf einer Platte bis zu mehreren Hundert Mikroelektroden, deren Messungen dann die Aktivitäten ganzer Netzwerke von Nervenzellen erfassen können. Mit diesen Sonden registrieren Forscher nicht nur die Ströme vereinzelter Nervenzellen in Kulturschalen. Sie werden häufig auch bei Versuchstieren fest implantiert und liefern dann über längere Zeit Daten, die beispielsweise auf die Veränderung von Netzwerken beim Lernen schließen lassen.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
Vor– und Nachteile
Mit Mikroelektroden lässt sich direkt die elektrische Aktivität einzelner Nervenzellen messen. Die zeitliche Auflösung ist dabei sehr hoch: Aktionspotenziale dauern oft nur wenige Millisekunden. Die räumliche Auflösung wird einerseits von der Größe der Elektrodenspitze definiert, darüber lassen sich andererseits noch keine Informationen ableiten. Zum Teil kontrollieren sie die Position daher mit anderen Methoden, etwa per Mikroskop (s.u.).
Die typische elektrische Antwort einer Nervenzelle, das Aktionspotenzial, folgt dem Muster: ganz oder gar nicht. Damit ist die Messung dieser Spannungsspitzen eine eindeutige Anzeige dafür, ob gerade ein Reiz verarbeitet wird oder nicht.
Klar ist allerdings auch: Für diese Messungen müssen Elektroden mitten ins Gewebe hineingestochen werden. Beim Menschen verbietet sich das von alleine ¬– außer bei der Diagnose oder Therapie etwa von Epilepsie oder Parkinson. Aber auch an lebenden Tieren sind zumindest Messungen im Zellinneren schwierig, denn allein schon die leichten Bewegungen, etwa beim Atmen, verschieben die Elektrode immer wieder. Im lebenden Organismus arbeiten Wissenschaftler daher vor allem mit extrazellulären Drahtelektroden.
Und die Forscher müssen schon im Voraus ziemlich genau wissen, welche Zelle sie untersuchen wollen und woran sie sie erkennen. Für den umgekehrten Weg – zu einer bestimmten Funktion die beteiligten Zellen zu suchen – eignet sich die Methode deutlich schlechter. Zu hoch ist der zeitliche Aufwand, immer wieder den Kontakt mit neuen Kandidatenzellen herzustellen, und zu sehr leidet unter den wiederholten Einstichen am Ende doch das ganze Netzwerk.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
Aktionspotenzial
Aktionspotenzial/-/action potential
In erregbaren Zellen (z. B. Neuronen oder Muskelzellen) findet man sehr schnelle Änderungen des elektrischen Potenzials über der Zellmembran. Dieses Ereignis ist die Grundlage für die Informationsleitung entlang des Axons der Nervenzelle. Das Aktionspotenzial setzt sich entlang der Zellmembran fort und entsteht nach dem Alles-oder-Nichts-Prinzip nur dann, wenn die Zelle ausreichend stark erregt wurde.
Empfohlene Artikel
Kombinationsmöglichkeiten
Ohne Kontrolle per Mikroskop würde die Messung mit Mikroelektroden in den seltensten Fällen Sinn ergeben. Schließlich will man nicht einfach blind in der grauen Masse herumstochern, nur um mit Glück das Verhalten irgendeiner beliebigen Nervenzelle aufzunehmen. Stattdessen steuern die Forscher mit ihren Mikroelektroden gezielt Zellen an, die sie wiedererkennen können – entweder, weil die Anatomie bekannt ist, oder indem sie nach der elektrischen Untersuchung durch die Pipette auch ein Färbemittel in die Nervenzelle spritzen.
Auch mit der Gentechnik geht die Elektrophysiologie per Mikroelektrode oft Hand in Hand. Die Frage lautet dann: Wie ändert sich die elektrische Signalverarbeitung, wenn bestimmte Moleküle in den Nervenzellen, und besonders an ihren Kontaktstellen, den Synapsen, gezielt verändert sind?
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
Ausblick
So spannend der Einblick in einzelne elektrisch aktive Nervenzellen ist – eine einzelne Nervenzelle macht noch kein Gehirn. Und sie ist vermutlich auch nicht alleine dafür verantwortlich, ein bestimmtes Gesicht oder Konzept zu speichern (siehe hier). Deshalb interessiert Forscher vermehrt die Aktivität des umgebenden Netzwerks. Immer mehr verbreitet sich daher die Arbeit mit Multielektrodenarrays. Gleichzeitig werden die Herstellungstechniken immer raffinierter, Verstärkersysteme und die Computer zur Analyse werden immer leistungsfähiger: So können die Signale von immer mehr Elektroden gleichzeitig ausgelesen werden.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
Neuron
Neuron/-/neuron
Das Neuron ist eine Zelle des Körpers, die auf Signalübertragung spezialisiert ist. Sie wird charakterisiert durch den Empfang und die Weiterleitung elektrischer oder chemischer Signale.
zum Weiterlesen:
- Microelectrode techniques, The Plymouth workshop handbook. Edited by D.C. Ogden, Company of Biologists, Cambridge, UK, 1994. [oder: www.utdallas.edu/~tres/microelectrode/me.html]
- Schwiening, CJ: A brief historical perspective: Hodgkin and Huxley. J Physiol. 2012 Jun 1; 590(Pt 11): 2571 – 2575. [dx.doi.org/10.1113/jphysiol.2012.230458]