Mikroskopie
Die Hirnforschung nutzt verschiedene wissenschaftliche Methoden. Hier stellen wir Ihnen zentrale Arbeitstechniken vor. Zum Beispiel die Mikroskopie.
Wissenschaftliche Betreuung: Dr. Katrin Willig
Veröffentlicht: 28.01.2016
Niveau: mittel
- Hirnforscher verwenden Licht- und Elektronenmikroskope. Erstere erlauben den Blick ins lebende Gehirn, letztere haben eine mit Lichtmikrospkopie unerreichbare Auflösung und ermöglichen die automatisierte und relativ schnelle Kartierung des gesamten Denkorgans.
- Im 19. Jahrhundert schon untersuchte Camillo Golgi mit einem Lichtmikroskop die Verbindungen zwischen Nervenzellen. Alois Alzheimer kam mit dem Instrument der nach ihm benannten Krankheit auf die Spur.
- Funktionen wie Erinnern oder Krankheiten wie Multiple Sklerose sollen durch den mikroskopischen Blick auf lebendes Gehirngewebe sowie den Vergleich des Konnektoms von gesundem und krankem Hirngewebe besser verstanden werden.
- Allerdings können herkömmliche Mikroskope nur circa einen Millimeter tief in lebendes Hirngewebe schauen. Eine Methode mit dem rätselhaften Namen "Optische Zeitumkehr" soll das ändern.
Lange galt für Lichtmikroskope die sogenannte Beugungsgrenze als maximale mögliche Auflösung: Alles, was größer war als 200 Nanometer, konnte dargestellt werden – alles darunter verschwamm zu einem undeutlichen Flecken. Dem Forscher Stefan Hell vom Max-Planck-Institut für biophysikalische Chemie in Göttingen gelang es 1999 nun mit einem Trick, diese 200 Nanometer bei einer speziellen Technik der Fluoreszenzmikroskopie zu unterschreiten. Für diese Arbeit an der sogenannten STED-Mikroskopie oder Nanoskopie bekam er zusammen mit Kollegen den Nobelpreis für Chemie 2014.
„Mit Licht kann man nicht nur ein Molekül anregen, sondern auch ein angeregtes Molekül schlagartig abregen“, erklärt Hell. Dies nennt man Stimulierte Emission. „Damit lässt sich Fluoreszenzlicht sehr gut von dem stimulierten oder dem stimulierenden Licht trennen. Abgeregte Moleküle können sofort wieder angeregt und von neuem abgeregt werden; der Prozess ist reversibel.“
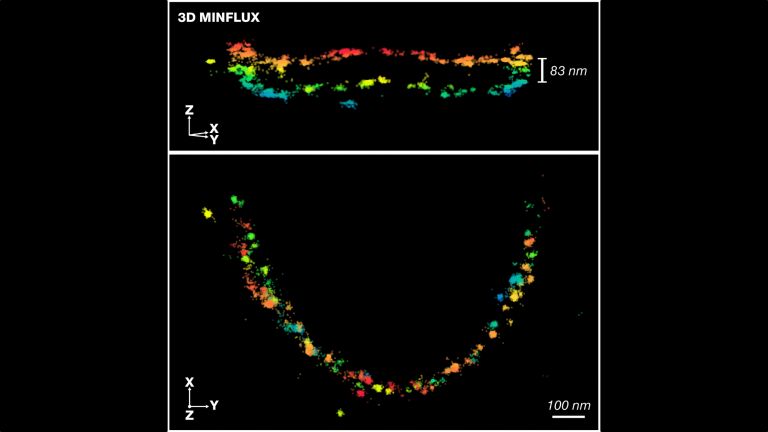
Konkret nutzte Hell diesen Prozess nun für den Bau eines besonderen Mikroskops. Ein Laser, der Anregungsstrahl, regt die fluoreszierenden Marker zum Leuchten an. Ein zweiter Laser, wie ein Ring um den ersten gelegt, regt sie wieder ab. So können letztlich nur die Marker im Zentrum des Anregungsstrahls leuchten – und dieses Zentrum ist je nach Lichtstärke des Laserrings um ihn herum deutlich geringer als 200 Nanometer. Fährt der Laser so die Probe ab, registriert er nacheinander Bereiche unterhalb der Beugungsgrenze und schafft so ein Abbild der Zellen. Inzwischen gelang Hell und Kollegen eine Auflösung von 2,4 Nanometern. Auch die Aufnahme von dynamischen Prozessen in Videos ist mit dieser Technik möglich. Erste Experimente gewährten bereits Einblicke in das Gehirn von lebenden Mäusen. Die Auflösung von Elektronenmikroskopen von etwa 0,1 Nanometer wurde bislang aber noch nicht erreicht.
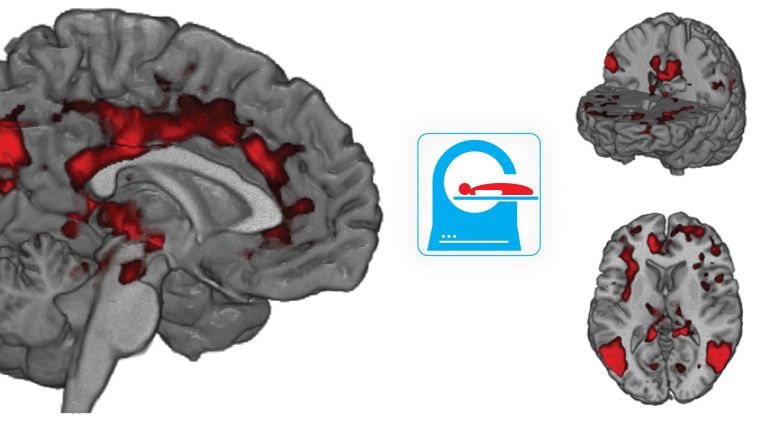
Dieses Gerät war das Attribut eines der bekanntesten Hirnforscher überhaupt: „Irrenarzt mit dem Mikroskop“ wurde Alois Alzheimer von seinen Zeitgenossen genannt. Seit Alzheimer haben Forscher einen ganzen Strauß an Spezialmikroskopen entwickelt, die tief in Aufbau und Arbeitsweise des Denkorgans blicken lassen. Mikroskope erlauben einen sehr viel feinkörnigeren Blick auf Nervenzellen und die Verbindungen zwischen ihnen als etwa die Magnetresonanztomografie. Der mikroskopische Blick auf das Denkorgan schafft neues Wissen über Funktionen des Gehirns wie das Lernen sowie über Krankheiten wie Demenz.
Demenz
Demenz/Dementia/dementia
Demenz ist ein erworbenes Defizit kognitiver, aber auch sozialer, motorischer und emotionaler Fähigkeiten. Die bekannteste Form ist Alzheimer. „De mentia“ bedeutet auf Deutsch „ohne Geist“.
Funktionsweise
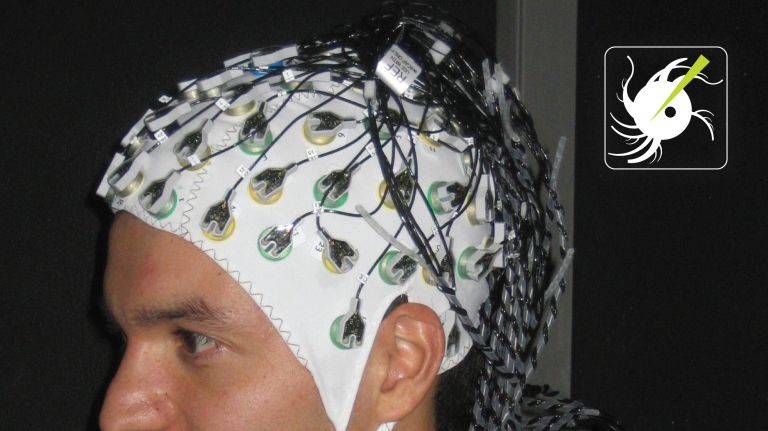
Die Hirnforschung verwendet zwei Arten von Mikroskopen: Licht– und Elektronenmikroskope: Mit Lichtmikroskopen lassen sich lebende Zellen und Nervengewebe untersuchen. Sie führen vom Untersuchungsobjekt reflektiertes sichtbares Licht durch ein System aus optischen Linsen, das ein stark vergrößertes Abbild erzeugt. Ein Maß für die Leistung eines Mikroskops ist das so genannte Auflösungsvermögen, welches den Mindestabstand angibt, den zwei Einzelobjekte, etwa zwei Lagen einer Membran, auseinander liegen müssen, um als solche abgebildet zu werden – und nicht als verwaschene Einheit. Das Auflösungsvermögen wird durch die Wellenlänge des verwendeten Lichts begrenzt und kann daher nicht besser sein als rund 200 Nanometer (Millionstel Millimeter). Man spricht von der so genannten Beugungsgrenze. Das Lichtmikroskop bildet daher größere Komponenten der Zellen ab, etwa den Zellkern oder die Zellmembran, während kleinere Objekte, etwa die innere Struktur von Mitochondrien, Viren oder das Erbmolekül DNA die Auflösungsgrenze unterschreiten. Mit einer Weiterentwicklung der Lichtmikroskopie, der so genannten STED-Mikroskopie, gelang es dem Forscher Stefan Hell vor einigen Jahren als erstem, diese Grenze zu unterschreiten (siehe Infokasten). Dafür bekam er den Nobelpreis für Chemie 2014.
Das Elektronenmikroskop verwendet statt sichtbarem Licht Strahlen von sehr schnellen Elektronen. So genannte elektronenoptische Linsen lenken die Elektronenstrahlen mittels elektrischer und magnetischer Felder auf analoge Weise ab wie optische Linsen die Lichtstrahlen. Laut Quantenphysik verhalten sich Elektronenstrahlen nämlich wie Lichtstrahlen, nur mit einer wesentlich kleineren Wellenlänge. Daher haben Elektronenmikroskope ein wesentlich größeres Auflösungsvermögen: weniger als ein Nanometer, sodass selbst Moleküle abgebildet werden können, etwa DNA oder Proteine.
Beim Elektronenmikroskop liegt das Objekt der Betrachtung in einer Vakuumkammer, in der äußerst tiefe Temperaturen herrschen. Nervenzellen oder –gewebe überleben darin nicht. Dafür ist die räumliche Auflösung eines Elektronenmikroskops sehr viel höher als die eines Lichtmikroskops; sie erreicht 0,1 Nanometer. Statt mit Linsen funktioniert das Elektronenmikroskop grob gesagt mit elektrischen und – beziehungsweise – oder magnetischen Feldern. Stark beschleunigte Elektronen werden auf das Objekt geleitet. Je nach Beschaffenheit des Materials dringen sie hindurch, werden abgelenkt oder reflektiert und treffen schließlich auf eine Art elektronischen Detektor. Helle Stellen zeigen an, dass Elektonen durchgelassen wurden, dunkle das Gegenteil. So entsteht ein Schwarz-Weiß-Abbild des Zellpräparats, das durch magnetische Objektive vergrößert und am Computerbildschirm sichtbar wird. Eine für die Hirnforschung wichtige Variante der Elektronenmikroskopie lenkt gleichzeitig viele Elektronenstrahlen auf die Probe. Diese „multi-beam“ genannte Methode erlaubt es, in kurzer Zeit großflächige Schnitte durch Hirngewebe vergrößert aufzunehmen.
Einsatzgebiete
Die hohe räumliche Auflösung und der Blick auf lebendes Hirngewebe machen Lichtmikroskope zu einem mächtigen Instrument der Hirnforschung. Man kann mit ihnen Aufbau und Funktion einzelner Zellen und Zellbestandteile, die Signalübertragung und die Vernetzung zwischen Nervenzellen erkunden.
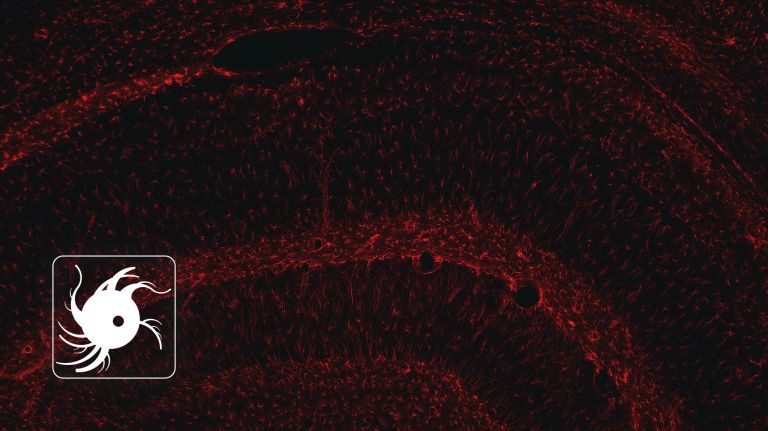
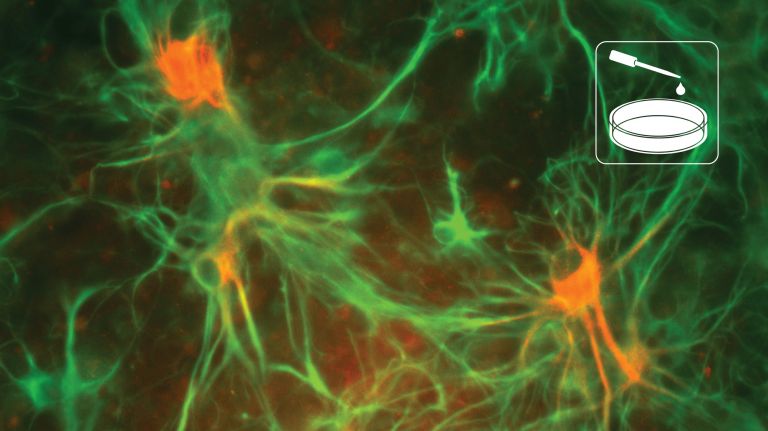
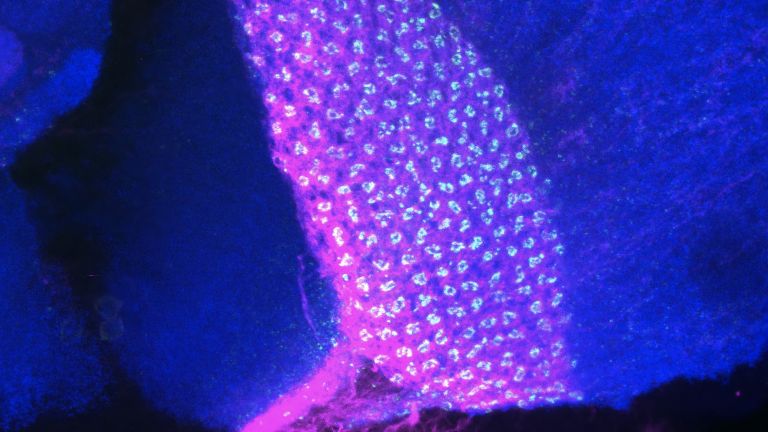
Um die jeweiligen Gewebearten besser sichtbar zu machen, werden die Untersuchungsobjekte häufig eingefärbt. Die so genannte Fluoreszenzmikroskopie – eine Teildisziplin der Lichtmikroskopie - wirkt wie ein Filter, die nur die interessierenden Objekte zeigt und alles andere ausblendet. Hierzu verwendet man Antikörper, die sich nur an bestimmte Zellbestandteile, etwa Proteine, binden. Diesen Antikörpern wurden vorab Farbstoffe beigefügt, die mit Laserlicht zum Leuchten in einer bestimmten Farbe angeregt werden können. Filter vor dem Okular des Mikroskops sorgen dafür, dass nur diese Farbe und damit nur die markierten Zellkomponenten sichtbar werden. Farbstoffe zum Beispiel, die nur in aktiven Nervenzellen zum Leuchten angeregt werden, verraten den Wissenschaftlern, wann und wie stark eine Zelle elektrisch aktiv ist.
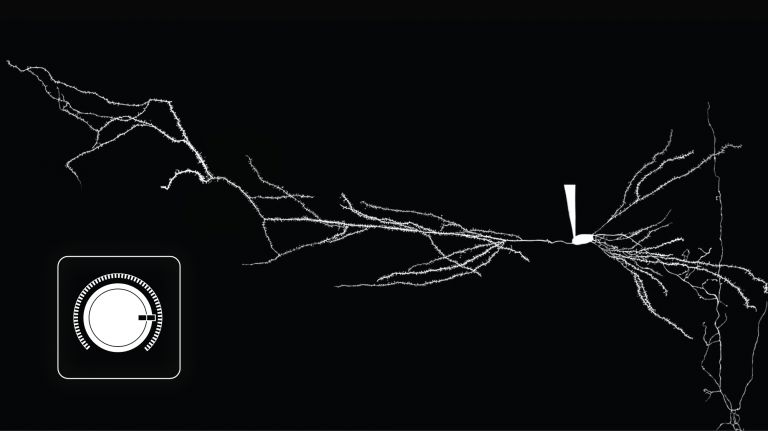
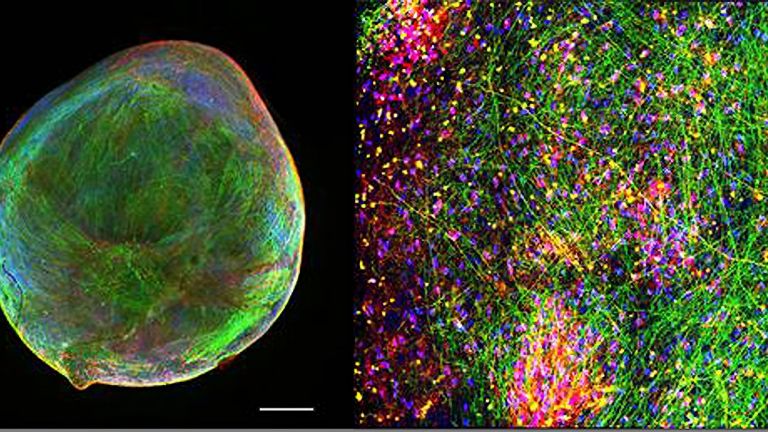
Mit der 2-Photonen-Mikroskopie lassen sich dreidimensionale Bilder aufnehmen. Die Aufnahmen haben eine räumliche Auflösung von etwa einem Mikrometer (tausendstel Millimeter), was etwa der Größe einer Synapse entspricht. Das Mikroskop verwenden Neuroforscher, um das Gehirn in Aktion zu beobachten, etwa die Reaktion des Neuronen-Netzwerks auf Umweltreize. Wissenschaftler vom Max-Planck-Institut (MPI) für Neurobiologie in Martinsried erforschen so zum Beispiel, wie sich Lernreize auswirken. So beobachteten sie, dass sich durch Lernen Stärke und Anzahl von Synapsen verändern. Auch Hirnkrankheiten kommen Neurowissenschaftler durch die Lebendbeobachtung von Nervengewebe auf die Spur. So fanden Forscher der Uni Mainz, dass bei Multipler Sklerose fehlgeleitete Immunzellen die Nervenzellen direkt angreifen.
Ein Zukunftsprojekt der Hirnforschung für die nächsten Jahrzehnte soll mit eigens entwickelten elektronenmikroskopischen Verfahren bewältigt werden: Die Erstellung des so genannten Konnektoms, eine allumfassende Kartierung des Gehirns mit allen Verbindungen zwischen den Nervenzellen.
Synapse
Synapse/-/synapse
Eine Synapse ist eine Verbindung zwischen zwei Neuronen und dient deren Kommunikation. Sie besteht aus einem präsynaptischen Bereich – dem Endknöpfchen des Senderneurons – und einem postsynaptischen Bereich – dem Bereich des Empfängerneurons mit seinen Rezeptoren. Dazwischen liegt der sogenannte synaptische Spalt.
Historie
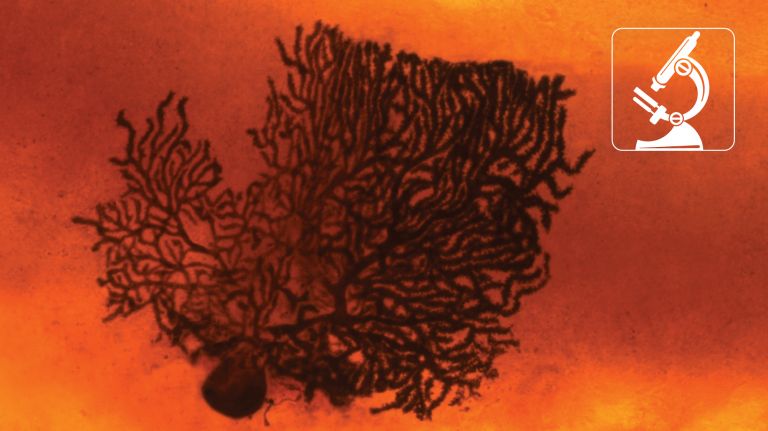
Pioniere der Hirnforschung setzten Mikroskope bereits im späten 19. Jahrhundert ein. Der italienische Mediziner Camillo Golgi färbte Nervengewebe mit Silbernitrat, sodass sich unter dem Mikroskop einzelne Nervenstränge verfolgen ließen. Alois Alzheimer fand unter dem Mikroskop jene als Plaques bezeichneten Eiweißablagerungen zwischen den Nervenzellen, die für die nach ihm benannte Krankheit typisch sind.
Plaques
senile Plaques/-/senile plaques
Senile Plaques lagern sich in der grauen Hirnsubstanz ab, wenn ein Eiweiß – das so genannte Amyloid-Vorläuferprotein – nicht korrekt abgebaut wird. Entzündungen sowie Erkrankungen des Fett– oder des Zuckerstoffwechsels können die Plaquebildung begünstigen. Im Schnitt erreichen die Ablagerungen einen Durchmesser von 50 Mikrometern. Das Auftreten von Plaques ist eine von mehreren anatomischen Veränderungen im Gehirn, anhand derer Pathologen nach dem Tod eine Alzheimer-Erkrankung diagnostizieren können.
Empfohlene Artikel
Vor– und Nachteile
Mikroskope liefern deutlich feinkörnigere Bilder als andere Untersuchungsmethoden der Hirnforschung, etwa die Magnetresonanztomografie. Vorgänge auf der Ebene einzelner Synapsen lassen sich beobachten. Die farbliche Markierung von bestimmten Zellbestandteilen bei der Fluoreszenzmikroskopie ist ein weiterer Vorteil, da sich diese Zellkomponenten dann selektiv beobachten lassen und sich somit einzelne Objekte und deren Funktion innerhalb eines komplexen Gesamtgeschehens studiert werden können. Doch Lichtmikroskope dringen in der Regel nur recht begrenzt in das Gewebe vor. Mit der Lichtmikroskopie lässt sich maximal ein 20-stel Millimeter tief unter die Oberfläche in ein lebendes Gehirn blicken, denn das Gewebe streut das Licht, wodurch es entlang seines Weges immer weiter abgeschwächt wird.
Deutlich tiefer, nämlich rund einen Millimeter ins Gewebe, reicht eine Variante der Fluoreszenzmikroskopie, die der Physiker Winfried Denk, heute am Max-Planck-Institut für Neurologie, zusammen mit Kollegen von der Cornell University im US-Staat New York vor rund 25 Jahren entwickelt hat. Dabei wird Licht mit der doppelten Wellenlänge als üblich eingestrahlt. Dadurch wird es sehr viel weniger gestreut und kann tiefer eindringen. Dieses Licht hat weniger Energie und schädigt daher das Gewebe auch weniger stark. Den Farbstoff regt es trotzdem zum Leuchten an, und zwar wenn ein Farbstoffmolekül zwei Lichtteilchen gleichzeitig absorbiert und daher die gleiche Energie aufnimmt wie durch das energiereichere Licht mit ursprünglicher Wellenlänge. Dennoch gilt: Tiefere Hirnstrukturen wie etwa der Mandelkern entziehen sich bislang dem mikroskopischen Blick der Forscher.
Nachteilig an der Elektronenmikroskopie ist die aufwändige Präparierung der Untersuchungsobjekte. Diese müssen zudem sehr dünn geschnitten werden, damit die Elektronen durch sie hindurch gelangen können.
Ausblick
Tiefer ins Gehirn soll eine Methode mit dem rätselhaften Namen „Optische Zeitumkehr“ blicken, die derzeit der Physiker Benjamin Judkewitz an der Berliner Charité entwickelt Judkewitz auf der NWG-Tagung im Interview. Am zu untersuchenden Punkt im Gewebe fokussiert das Berliner Team ein Ultraschallsignal. Dann sendet es Licht durch die Probe. Am Brennpunkt des Ultraschalls wird seine Frequenz leicht verändert. Den Strahl mit der modifizierten Frequenz reflektiert ein Spezialspiegel auf der anderen Seite der Probe. Er läuft dann den gleichen Weg rückwärts. Das Licht passiert den Brennpunkt wieder und trägt somit ein zweites Mal zur dortigen Lichtintensität bei. Das wirkt sozusagen wie eine Fackel, die tiefer liegende Gewebe sichtbar macht. „Wir streben langfristig an, die Eindringtiefe zu verdoppeln“, sagt Judkewitz. Für den Einsatz im Gehirn ist die Methode jedoch noch nicht reif.
Funktionen des Gehirns wie Lernen und Erinnerung oder die Entstehung von Krankheiten sollen auch durch das Studium des Konnektoms besser verstanden werden, etwa durch den Vergleich von gesunden und kranken neuronalen Netzwerken. Ein Team um Winfried Denk vom MPI in Martinsried entwickelte dazu eine Methode, mit der ein gesamtes Maushirn eingefärbt wird. Ein Roboter soll das Organ dann in hauchdünne Schichten zerschneiden und nacheinander in einem Multi-beam-Elektronenmikroskop untersuchen. Alle Zellen und Verbindungen zwischen ihnen sollen so erfasst und anschließend in einem Computer zu einem vollständigen 3D-Bild des Gehirns zusammengesetzt werden.
In den nächsten drei Jahren wollen die Martinsrieder Forscher die Daten erfassen. Die Erstellung des 3D-Bildes, für die die Methoden erst noch entwickelt werden, folgt darauf. Das rund 3000 Mal größere Konnektom eines menschlichen Hirns mit seinen fast 1000 Billionen Verbindungen aufzunehmen, die Daten zu speichern und zu analysieren sei derzeit allerdings noch „Science Fiction“, wie das Martinsrieder Institut mitteilt.
Jedenfalls zeigen die Neuentwicklungen, dass die Hirnforschung noch viel von Mikroskopie erwarten darf.