Legalize it?! Was bringt Cannabis medizinisch?

Cannabis begleitet den Menschen schon seit langer Zeit. Auch wenn viele auf cannabinoidhaltige Substanz schwören, wird ihr medizinischer Nutzen unter Experten kontrovers diskutiert.
Wissenschaftliche Betreuung: Prof. Dr. Dieter K. Meyer, Prof. Dr. Rainer Spanagel
Veröffentlicht: 11.12.2025
Niveau: mittel
- Die Hanfpflanze begleitet den Menschen schon lange, auch als Heilmittel. Durch das Cannabis-Gesetz von 2017, wurden cannabishaltige Präparate in den Leistungskatalog der Krankenkassen aufgenommen, ihre legale Nutzung damit erleichtert. Nicht alle Mediziner sind davon allerdings erfreut.
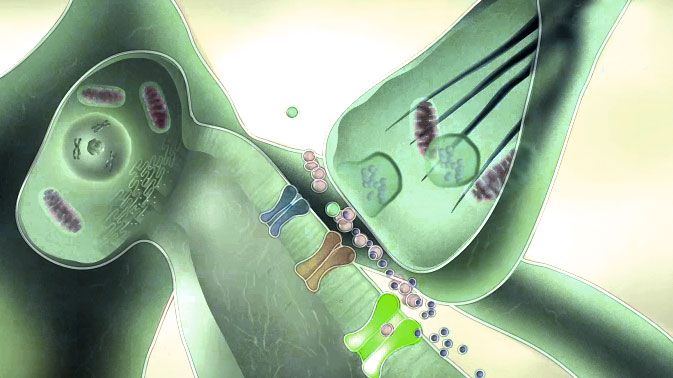
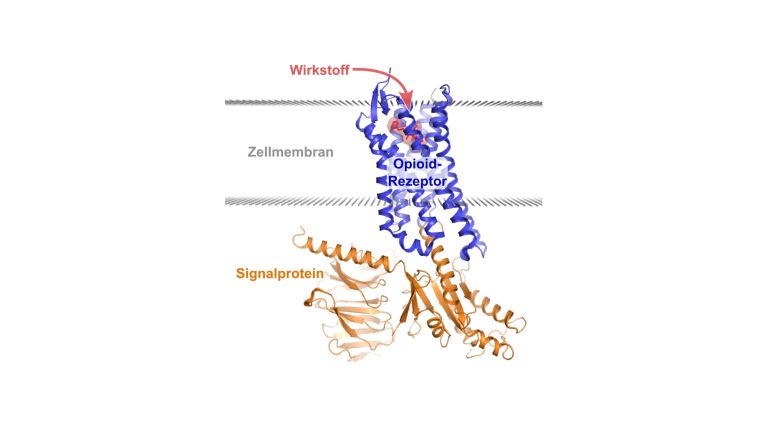
- Wirkstoffe aus der Hanfpflanze, wie zum Beispiel THC oder CBD, docken im Körper an die Cannabinoid-Rezeptoren CB1 und CB2 an. Körpereigene Botenstoffe, welche diese Bindungsstellen aktivieren, heißen Endocannabinoide. Zusammengenommen bilden sie das Endocannabinoid-System.
- Das Endocannabinoid-System (ECS) ist gut charakterisiert – es beeinflusst unser emotionales Verhalten, Motivations- und kognitive Prozesse. Außerdem ist das ECS in eine Vielzahl von physiologischen Prozessen involviert. Dazu gehören beispielsweise Immunfunktion, Appetitregulierung, und Schmerzwahrnehmung. Auch bei der Entwicklung des Nervensystems spielt es eine wichtige Rolle.
- Mediziner dürfen cannabishaltige Medikamente verschreiben, falls andere Präparate nicht ausreichend gewirkt haben oder passende Alternativen nicht zur Verfügung stehen. Sie haben damit einen großen Ermessensspielraum.
- Klinische Studien deuten auf die Wirksamkeit von Cannabispräparaten bei einigen Erkrankungen wie chronischen Schmerzen hin. CBD ist als Epidolex zugelassen und hochwirksam bei kindlichen Epilepsien wie dem Lennox-Gastaut-Syndrom oder dem Dravet-Syndrom. Allerdings ist der Zusatznutzen bei vielen anderen Erkrankungen selbst unter Fachleuten weiterhin umstritten.
- Zu den akuten Nebenwirkungen von cannabishaltigen Präparaten zählen Müdigkeit, Schwindel oder Euphorie – aber auch Angst oder Panik können auftreten. Über langfristige Folgen ist weniger bekannt, allerdings gibt es Hinweise auf reduzierte kognitive Fähigkeiten und ein erhöhtes Risiko von psychischen Erkrankungen bei empfänglichen Personen. Insbesondere steigt das Psychose Risiko erheblich bei dem Konsum von hochdosierten Cannabisprodukten. Weil das Endocannabinoid-System eine Rolle bei der Entwicklung des Nervensystems spielt, warnen Experten insbesondere Jugendliche vor einem unbedachten Konsum. Kognitive Fähigkeiten können bei hohem Cannabiskonsum im Jugendalter bleibend beeinträchtigt werden.
- Es bedarf noch weiterer kontrollierter Studien, um das vollständige Profil von cannabishaltigen Produkten besser verstehen zu können. Dazu sollte auch eine bessere Erforschung der biologischen Mechanismen von THC und CBD gehören.
Die Hanfpflanze und ihre Extrakte begleiten den Menschen schon seit langer Zeit. In vielen alten Kulturkreisen wurde Cannabis seit Jahrtausenden zu medizinischen und rituellen Zwecken genutzt. In Europa fand der therapeutische Einsatz bereits im 19. Jahrhundert breite Anwendung, zum Beispiel bei der Behandlung von Schmerzen. Danach geriet die Hanfpflanze und ihre medizinische Anwendung im Westen allerdings zunehmend in Vergessenheit – allerdings nicht zwangsläufig ihre „nicht-therapeutische“ Wirkungen –, aus der die Hanfpflanze und ihre Extrakte seit einiger Zeit langsam zu erwachen scheinen. Unter Experten ist ihr medizinischer Nutzen aber alles andere als unumstritten.
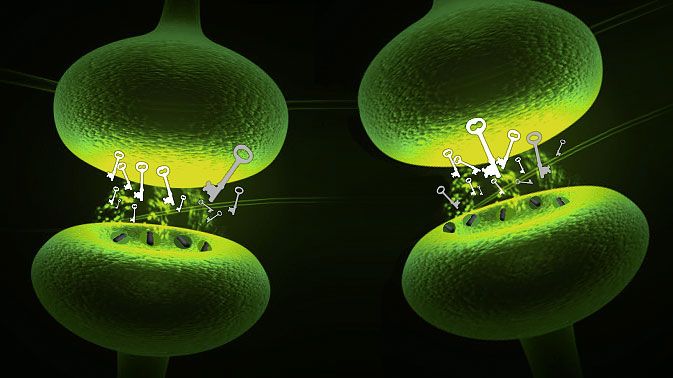
Noch nicht ganz so lange ist es her, dass die biologische Ursache für die vielfältige Wirkung von Cannabinoiden entschlüsselt wurde. Um 1990 fand man heraus, dass die psychoaktive Substanz Tetrahydrocannabinol, genauer gesagt 9- Tetrahydrocannabinol – besser bekannt als THC oder Dronabinol, dem internationalen Freinamen – an spezielle Cannabinoid-Rezeptoren im Gehirn bindet. Da wenig plausibel schien, dass die Evolution im Gehirn ein Schloss eigens für einen Schlüssel hervorbringt, der nur in der Hanfpflanze zu finden ist, machte man sich auf die Suche nach körpereigenen Bindungspartnern, den „endogenen Cannabinoiden“. Als erste derartige Substanz konnte man 1992 aus Schweinehirnen Anandamid isolieren, dessen Name sich vom Sanskrit-Wort für „inneres Entzücken“ herleitet. Mittlerweile weiß man, dass das Endocannabinoid-System aus zwei verschiedenen Cannabinoid-Rezeptoren (CB1 und CB2) besteht. Diese sind über das zentrale und periphere Nervensystem verstreut und beeinflussen wichtige körperliche Prozesse wie beispielsweise Immunfunktion, Appetitregulierung, Gedächtnis und Schmerzwahrnehmung. Auch bei der Entwicklung des Nervensystems und im Jugendalter spielt das Endocannabinoid-System eine wichtige Rolle. So finden sich während der Adoleszenz deutlich mehr CB1 Rezeptoren als Im Erwachsenalter.
THC ist aber nicht der einzige Wirkstoff der Hanfpflanze. Eine weitere (unscheinbarere) Substanz ist das Cannabidiol (CBD). Es entfaltet seine Wirkung ebenfalls über Cannabinoid-Rezeptoren, allerdings oftmals mit THC entgegengesetzten Effekten. CBD ist nicht psychoaktiv und macht auch nicht „high“ – deswegen unterliegt CBD, anders als THC, auch nicht dem Betäubungsmittelgesetz (BtMG). Die krampflösende Wirkung bei kindlichen Epilepsieformen ist sehr gut belegt und findet klinische Anwendung. Ob CBD entzündungshemmend und antipsychotisch wirken, ist nach wie vor nicht abschließend geklärt.
Gedächtnis
Gedächtnis/-/memory
Gedächtnis ist ein Oberbegriff für alle Arten von Informationsspeicherung im Organismus. Dazu gehören neben dem reinen Behalten auch die Aufnahme der Information, deren Ordnung und der Abruf.
THC: Alter Wein in neuen Schläuchen?
Mit dem Mundspray Nabiximols (Handelsname Sativex) wurde 2011 das erste Medikament auf Cannabisbasis in Deutschland zugelassen. Es beinhaltet ein standardisiertes Cannabisextrakt aus THC und CBD im Verhältnis von 1:1 und ist für die Behandlung von spastischen Beschwerden bei Patienten mit Multipler Sklerose vorgesehen. Seitdem ist mit Nabilon (Handelsname Canemes) ein weiterer Wirkstoff auf Cannabisbasis zugelassen worden. Bis zum 10.03.2017 wurde die Verschreibung von cannabishaltigen Medikamenten allerdings dadurch erschwert, dass Krankenkassen eine Kostenübernahme ablehnen durften. Zwar konnten Mediziner Präparate wie Sativex im Rahmen eines individuellen Heilversuchs verschreiben – allerdings mit dem Risiko, dass die Patienten auf den Kosten sitzenblieben. Mit dem so genannten Cannabis-Gesetz wurde die Übernahme der Behandlungskosten in die Leistungskataloge der Krankenkassen aufgenommen. Für viele Ärzte ergeben sich damit allerdings mehr Fragen als Antworten.
Cannabinoid-haltige Medikamente richten sich in der Regel an Patienten, bei denen konventionelle Therapien nicht ausreichend anschlagen. Allerdings räumt das Gesetz den Ärzten hier einen großen Ermessensspielraum ein, da es keine direkten Vorgaben zu den zugelassenen Indikationen macht. Damit bleibt es dem Arzt überlassen, wo „eine allgemein anerkannte, dem medizinischen Standard entsprechende Leistung im Einzelfall nicht zur Verfügung steht“ oder „im Einzelfall nach der begründeten Einschätzung des behandelnden Vertragsarztes unter Abwägung der zu erwartenden Nebenwirkungen und unter Berücksichtigung des Krankheitszustandes der oder des Versicherten nicht zur Anwendung kommen kann“, wie es der Gesetzgeber formuliert. Hinweise auf eine Wirksamkeit fanden sich in kontrollierten Studien für Dronabinol vor allem bei der Behandlung von Spastik (z.B. bei Multipler Sklerose), Appetitlosigkeit und Übelkeit (z.B. während einer Chemotherapie) sowie chronischen Schmerzen (z.B. bei Rheuma). Allerdings ist dabei nicht aus den Augen zu verlieren, dass die Datenlage immer noch recht unsicher ist, unter anderem aufgrund fehlender oder suboptimaler klinischer Studien.
2025 wurde erstmals eine gut kontrollierte Phase III Studie zu einem Cannabisextrakt und der Wirksamkeit bei chronischem Rückenschmerz publiziert. Diese Studie könnte bald zu einer europäischen Zulassung führen – weltweit leiden 450 Millionen Menschen unter chronischem Rückenschmerz. Bisher behandelt man hauptsächlich mit Opiaten – auch das hat zur amerikanischen Opioidkrise beigetragen. Laut den Centers for Disease Control and Prevention (CDC) wurden in den letzten Jahren über 500.000 Todesfälle aufgrund von Opioidüberdosierungen registriert. Hier wäre als Alternative ein Cannabisextrakt ein Segen.
Empfohlene Artikel
Zeit für eine grundlegende Zulassung?
Unabhängig von der therapeutischen Wirksamkeit sind Cannabinoid-haltige Medikamente nicht harmlos. Zu den häufigsten akuten Nebenwirkungen zählen Müdigkeit, Schwindel, Herzrasen und gesteigerter Appetit. Außerdem löst insbesondere THC psychische Effekte wie Euphorie, eine veränderte Wahrnehmung und Entspannung aus – ebenfalls können allerdings Angst und Panik auftreten. Vieles hängt dabei ab vom Mischungsverhältnis THC zu CBD, das sich in den Züchtungen der vergangenen Jahre scheinbar zugunsten von THC verändert hat. Das Cannabis der Hippie-Bewegung der 60er Jahre ist also nur noch bedingt mit unserem heutigen vergleichbar. In den vergangen 50 Jahren hat der THC Gehalt sich um das fast 10-fache gesteigert. Dies ist Besorgnis erregend da mit höherem THC-Gehalt auch das Risiko auf eine Psychose enorm ansteigt.
Cannabishaltige Präparate können zudem zu einer Einschränkung von Gedächtnis und Motorik führen, was die Fahrtüchtigkeit beeinträchtigt. Da das Endocannabinoid-System eine wichtige Rolle bei der Entwicklung des Nervensystems spielt, kann Cannabiskonsum gerade für Jugendliche gravierende Risiken bergen.
Über die Langzeitwirkung von Cannabis-Wirkstoffen belegen Tierexperimente gravierende und bleibende Beeinträchtigungen. Im Humanbereich sind longitudinale Studien über die Lebensspanne enorm aufwendig und so gibt es nur wenig gesicherte Befunde. Eine bleibende Einschränkung der kognitiven Leistungsfähigkeit nach sehr hoher Dosierung ist möglich. Entzugssymptome, wie sie bei anderen Medikamenten beschrieben worden sind, stellen bei korrekter medizinischer Anwendung scheinbar eher selten ein Problem dar. Inwieweit Cannabispräparate allerdings eine „Einstiegsdroge“ für andere Substanzen darstellen (Gateway-Hypothese), wird weiterhin kontrovers diskutiert. Aktuelle Forschung legt nahe, dass die Beziehung zwischen Cannabiskonsum und dem Konsum anderer Drogen wie etwa Kokain nicht eindimensional betrachtet werden kann – hier spielt der Kontext aus umfassenderen sozialen und individuellen Variablen eine entscheidende Rolle. Aus Sicht vieler Forscher sollte die Gateway-Hypothese daher nicht als Argument gegen Cannabiskonsum politisch genutzt werden.
Mit Sicherheit haben cannabishaltige Medikamente Potenzial bei der Behandlung im Rahmen von bestimmten Erkrankungen. Allerdings bedarf es weiterer klinischer Studien, die hohen methodischen Ansprüchen genügen, um solche Vermutung zu untermauern. Das sollte vor allen Dingen zum Wohle der Patienten ohne Vorbehalte geschehen – und zwar von Befürwortern als auch Gegnern.
Wahrnehmung
Wahrnehmung/Perceptio/perception
Der Begriff beschreibt den komplexen Prozess der Informationsgewinnung und –verarbeitung von Reizen aus der Umwelt sowie von inneren Zuständen eines Lebewesens. Das Gehirn kombiniert die Informationen, die teils bewusst und teils unbewusst wahrgenommen werden, zu einem subjektiv sinnvollen Gesamteindruck. Wenn die Daten, die es von den Sinnesorganen erhält, hierfür nicht ausreichen, ergänzt es diese mit Erfahrungswerten. Dies kann zu Fehlinterpretationen führen und erklärt, warum wir optischen Täuschungen erliegen oder auf Zaubertricks hereinfallen.
Gedächtnis
Gedächtnis/-/memory
Gedächtnis ist ein Oberbegriff für alle Arten von Informationsspeicherung im Organismus. Dazu gehören neben dem reinen Behalten auch die Aufnahme der Information, deren Ordnung und der Abruf.
Erstveröffentlichung am 5. April 2018
Letzte Aktualisierung am 11. Dezember 2025