Das alternde Gehirn: Protein-Kartierung liefert neue Erkenntnisse
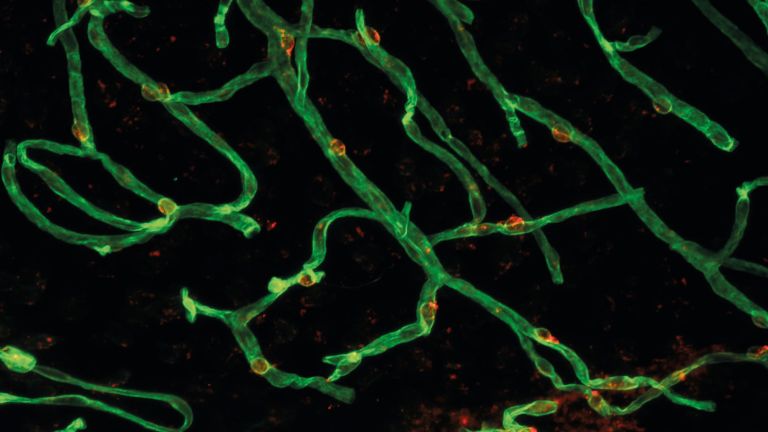
Forschende der LMU und des Exzellenzclusters SyNergy haben analysiert, wie sich das Proteom bestimmter Hirnzellen im Alter verändert.
Veröffentlicht: 22.03.2024
Damit die Nervenzellen im Gehirn reibungslos funktionieren und Informationen verarbeiten können, ist das zentrale Nervensystem auf eine streng kontrollierte Umgebung angewiesen. Diese wird durch die Blut-Hirn-Schranke aufrechterhalten: Spezialisierte Hirnendothelzellen sitzen an den Innenwänden der Blutgefäße und kontrollieren den Austausch von Molekülen zwischen Blut- und Nervensystem. Frühere Studien haben gezeigt, dass verschiedene von diesen Zellen abhängige Funktionen, wie die Integrität der Blut-Hirn-Schranke oder die Steuerung der Blutversorgung im Gehirn, im Laufe des Lebens abnehmen. Diese Fehlregulation führt zu Dysfunktionen in den Blutgefäßen und trägt damit entscheidend zu Erkrankungen wie Schlaganfall und Demenz bei.
Die molekularen Veränderungen, die diesem Funktionsverlust zugrunde liegen, sind bisher jedoch unzureichend bekannt. Um sie besser zu verstehen, untersuchen Forschende in molekularen Profiling-Studien die verschiedenen Bestandteile der Hirnendothelzellen und sammeln ihre Erkenntnisse in groß angelegten Datenbanken. „Das Transkriptom, also die in den Endothelzellen enthaltene RNA, ist inzwischen recht umfassend kartiert“, sagt LMU-Professor Martin Dichgans vom Institut für Schlaganfall- und Demenzforschung am LMU-Klinikum und einer der Verantwortlichen im Exzellenzcluster SyNergy . „Was bislang aber fehlte, sind entsprechende Daten zur Gesamtheit aller Proteine in den Zellen, dem sogenannten Proteom.“ Eine kürzlich im Fachmagazin Nature Aging publizierte Studie unter maßgeblicher Beteiligung von Forschenden der LMU und SyNergy schließt nun diese Wissenslücke.
"Unsere Ergebnisse zeigen Fehlregulationen von Schlüsselmolekülen bei der Stoffaufnahme in die Zellen, dem Rezeptorrecycling und dem Abbau von Stoffen im Lysosom." Martin Dichgans
Blut-Hirn-Schranke
Blut-Hirn-Schranke/-/blood brain barrier
Eine selektiv durchlässige Membran, die von den Zellen in den Wänden der kapillaren Blutgefäße im Gehirn gebildet wird. Sie schützt das Gehirn vor Schadstoffen über das Blut, erlaubt jedoch den Übergang von Nährstoffen und Sauerstoff aus dem Blut ins Gehirn.
Schlaganfall
Schlaganfall/Apoplexia cerebri/stroke
Bei einem Schlaganfall wird das Gehirn oder Teile davon nicht mehr ausreichend mit Blut versorgt, wodurch Sauerstoff- und Glukoseversorgung beeinträchtigt sind. Die häufigste Ursache ist ein Verschluss einer Arterie (ischämischer Schlaganfall), seltener eine Blutung (hämorrhagischer Schlaganfall). Typische Symptome sind plötzliche Sehstörungen, Schwindel, Lähmungen, Sprach- oder Sensibilitätsstörungen. Langfristige Folgen können verschiedene Gefühls-, Bewegungs- und kognitive Einschränkungen sein.
Demenz
Demenz/Dementia/dementia
Demenz ist ein erworbenes Defizit kognitiver, aber auch sozialer, motorischer und emotionaler Fähigkeiten. Die bekannteste Form ist Alzheimer. „De mentia“ bedeutet auf Deutsch „ohne Geist“.
Fehlregulierter Stoffwechsel
Dafür entwickelte das Team ein spezielles Protokoll zur Anreicherung von Hirnendothelzellen der Maus, mit dem altersabhängige Veränderungen in der Proteinzusammensetzung aufgelöst werden können. Anhand einer Clusteranalyse setzten die Wissenschaftlerinnen und Wissenschaftler diese Proteindynamik dann mit biologischen Funktionen in Verbindung. „Unsere Ergebnisse zeigen Fehlregulationen von Schlüsselmolekülen bei der Stoffaufnahme in die Zellen, dem Rezeptorrecycling und dem Abbau von Stoffen im Lysosom“, so Dichgans.
Zu den auffälligsten Veränderungen gehörte ein Rückgang von Proteinen, die am Vesikel-vermittelten Transport beteiligt sind. Außerdem liefert die Studie Belege dafür, dass ein Mangel des im Fettstoffwechsel relevanten Apolipoproteins E die Alterung beschleunigen kann. „Die Ergebnisse ergänzen und erweitern Erkenntnisse aus Studien zur RNA-Sequenzierung von Hirnendothelzellen im Verlauf des Alterns“, meint Dichgans. „Unser Proteomik-Ansatz erfasst z.B. Prozesse, die auf der RNA-Ebene nicht erkannt werden.“ Insgesamt biete die Studie einen Rahmen für das Verständnis wichtiger endothelialer Signalwege während der Alterung und diene als Datengrundlage für zukünftige Analysen der Gehirnendothel-Funktion. Ihre Daten zur altersabhängigen Proteinhäufigkeit des Maus-Endothels bieten die Forscherinnen und Forscher in einer öffentlich zugänglichen Datenbank zur weiteren Nutzung an.
Originalpublikation
Katalin Todorov-Völgyi, Judit González-Gallego et al: Proteomics of mouse brain endothelium uncovers dysregulation of vesicular transport pathways during aging. Nature Aging 2024