Das Protein-Kleid einer Nervenzelle
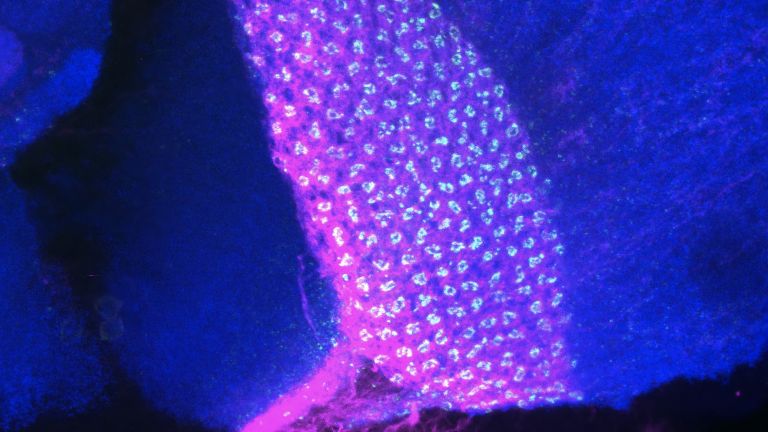
Neue Methode markiert Proteine und zeigt, in welche Rezeptoren sich Nervenzellen kleiden
Veröffentlicht: 28.10.2020
Wo in einer Nervenzelle befindet sich ein bestimmter Rezeptor? Ohne Antwort auf diese Frage ist es fast unmöglich, Rückschlüsse über die Funktion dieses Proteins zu ziehen. Zwei Wissenschaftlerinnen am Max-Planck-Institut für Neurobiologie haben eine Methode in der Fruchtfliege entwickelt, die Rezeptorproteine in ausgewählten Zellen markiert. Dadurch erlangten sie neue Einblicke in die neuronalen Mechanismen des Bewegungssehen. Doch zudem erhält die Forschungsgemeinschaft ein innovatives Werkzeug, mit dem sich Proteine jeglicher Art markieren lassen.
Eine der grundlegendsten Fragen der Neurobiologie ist, wie ankommende Sinneseindrücke in den Nervenzell-Schaltkreisen des Gehirns verarbeitet werden. Dabei ist es nicht nur wichtig zu verstehen, welche Nervenzellen durch Synapsen verknüpft sind, sondern auch wie diese miteinander kommunizieren. Hierbei spielen Rezeptoren eine entscheidende Rolle.
Diese speziellen Proteine sitzen in der Membranhülle von Nervenzellen an den Stellen, wo sie über Synapsen eintreffende Signale anderer Zellen aufnehmen. Je nach Rezeptor-Typ und Position bestimmen sie, wie die Zellen auf ankommende Informationen reagieren: Werden sie aktiviert oder gehemmt, und wie schnell geschieht dies? Um ein neuronales Netzwerk in seiner Gesamtheit zu verstehen ist es somit unerlässlich, Rezeptoren und ihre Verteilung in Nervenzellen zu untersuchen. Dies ist jedoch kein leichtes Unterfangen.
Einige etablierte Methoden geben keinen oder nur geringen Aufschluss über die Verteilung von Proteinen. Andere Techniken erlauben zwar das Markieren von künstlich in die Zellen eingebrachten Rezeptoren, aber nicht von natürlich vorkommenden. Die Doktorandinnen Sandra Fendl und Renee Vieira aus Alexander Borsts Abteilung nutzten die genetischen Methoden, die in der Fruchtfliege zur Verfügung stehen und entwickelten eine neue Methode zur Proteinmarkierung.
Mit der neuen Technik lassen sich zelleigene Rezeptoren mit dem grün fluoreszierenden Protein markieren – und das nur in ausgewählten Zellen. Letzteres ist essentiell, um innerhalb des dichten Nervenzell-Geflechts die markierten Rezeptoren den Zellen zuzuordnen, für die man sich interessiert.
Anhand dieser Methode analysierten die Wissenschaftlerinnen Rezeptoren in Nervenzellen, die im visuellen System der Fruchtfliege Bewegungen verarbeiten. Sie stellten fest, dass sich verschiedene Rezeptoren keineswegs zufällig entlang einer Nervenzelle anordnen. Selbst innerhalb eines Dendrits, dem Teil der Nervenzelle, der einkommende Signale aufnimmt, sind Rezeptorproteine ganz charakteristisch verteilt.
Mit einer Genauigkeit von nahezu einem Mikrometer zeigt die Studie so, welche Synapse entlang eines Dendrits auf welchen Rezeptor trifft. Dadurch lassen sich nun Aussagen über die Kommunikation einzelner Nervenzellverknüpfungen treffen. Dies liefert ein weiteres wichtiges Puzzlestück, um die neuronalen Schaltkreise im visuellen System der Fruchtfliege ganzheitlich aufzuschlüsseln.
Doch nicht nur das: die neue Methode lässt sich auch leicht und ohne großen Aufwand auf Tausende von anderen Proteinen erweitern. Somit können zukünftig unzählige Proteine in ausgewählten Zellen markiert und untersucht werden – und das geht weit über die spezifischen neurobiologischen Fragestellungen zum Bewegungssehen hinaus.
Synapse
Synapse/-/synapse
Eine Synapse ist eine Verbindung zwischen zwei Neuronen und dient deren Kommunikation. Sie besteht aus einem präsynaptischen Bereich – dem Endknöpfchen des Senderneurons – und einem postsynaptischen Bereich – dem Bereich des Empfängerneurons mit seinen Rezeptoren. Dazwischen liegt der sogenannte synaptische Spalt.
Rezeptor
Rezeptor/-/receptor
Ein Rezeptor ist ein meist membranständiges oder intrazelluläres Protein, das ein spezifisches externes Signal (z. B. einen Neurotransmitter, ein Hormon oder einen anderen Liganden) erkennt und die Zelle dazu veranlasst, eine definierte Antwort auszulösen. Je nach Rezeptortyp kann diese Antwort erregend, hemmend oder modulierend sein.
Originalpublikation
Sandra Fendl, Renee M. Vieira, Alexander Borst; Conditional protein tagging methods reveal highly specific subcellular distribution of ion channels in motion-sensing neurons; eLife, 20.10.2020; https://dx.doi.org/10.7554/eLife.62953